题目内容
20.给试管里的物质加热必须使用试管夹.试管夹应从试管的底部套入,夹在试管的中上部.若给试管里的液体加热,液体体积一般不超过试管容积的$\frac{1}{3}$,试管跟桌面成45°角.分析 根据试管夹的使用方法与实验室给试管内液体药品加热的正确操作方法分析即可.
解答 解:给试管里的物质加热必须使用试管夹.试管夹应从试管的底部套入,夹在离试管口$\frac{1}{3}$处.若给试管里的液体加热,液体体积一般不超过试管容积的$\frac{1}{3}$,试管跟桌面成45°角,先使试管均匀受热,然后小心地在试管里液体的底部加热,并且不时地左右移动试管.
故答案为:底部;$\frac{1}{3}$;45°角.
点评 给试管中的液体加热时一定要按正确的操作方法,以免液体飞溅而伤人,试管夹应夹在离试管口$\frac{1}{3}$处.

练习册系列答案
相关题目
11.按下列装置进行相关实验,其中不能达到目的是( )
| A. | 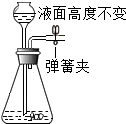 检查装置气密性 | B. | 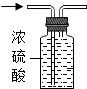 干燥O2 | C. | 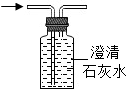 检验CO2 | D. | 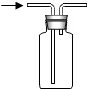 收集并储存H2 |
15.现有镁、铝、锌的混合物20g与适量的稀硫酸恰好完全反应,蒸发水后得到固体68g,如果将实验中用的稀硫酸改为稀盐酸,其他操作不变,蒸发后得到固体的质量为( )
| A. | 68g | B. | 91g | C. | 55.5g | D. | 无法确定 |
9.下列物质的用途中,主要应用其化学性质的是( )
| A. | 用铁铝制作饮具 | B. | 用干冰进行人工降雨 | ||
| C. | 用酒精作燃料 | D. | 用铜作导线 |