题目内容
3.向盐酸和氯化铜的混合溶液中加入过量的铁粉,充分反应后过滤,下列的有关实验叙述正确的是( )| A. | 反应中一定有气体产生 | B. | 滤液中含有CuCl2 | ||
| C. | 滤出的固体可能是纯净物 | D. | 溶液的质量一定减少 |
分析 根据金属活动顺序表中铁、铜的金属活动性强弱去作答,在金属活动性顺序中,这二种金属的金属活动性由强到弱的顺序为铁>氢>铜.在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,排在氢前面的金属可以和酸(稀盐酸和稀硫酸)反应放出氢气.
解答 解:
A、铁和盐酸反应放出氢气,故正确;
B、铁排在铜的前面,所以铁能将CuCl2中铜置换出来,又因为加入过量的铁粉,所以滤液中一定没有CuCl2,故错误;
C、铁能将CuCl2中铜置换出来,又因为加入过量的铁粉,所以滤出的固体中含有铜和铁,属于混合物,故错误;
D、铁与CuCl2反应生成铜和氯化亚铁,溶液质量减少;而铁和HCl反应生成氢气和氯化亚铁,溶液质量增加,所以最后溶液的质量不能够确定,故错误.
故选:A.
点评 本题考查了金属活动性顺序的应用,金属活动性顺序中位于氢之前的金属能从酸中置换出氢,活动性强的金属能将活动性弱的金属从其盐溶液中置换出来.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
12.当你使用复印机复印材料时,经常能闻到一股特殊的气味,这种气味是臭氧的气味,因为空气中的
氧气在放电条件下可以转化为臭氧.下列与此相关的说法中正确的是( )
氧气在放电条件下可以转化为臭氧.下列与此相关的说法中正确的是( )
| A. | 该变化是物理变化 | B. | 臭氧与氧气是同一种物质 | ||
| C. | 该变化是化学变化 | D. | 臭氧与氧气性质完全相同 |
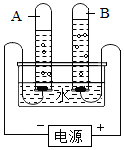 水是生命之源,爱护水资源是每个公民应尽的责任和义务.
水是生命之源,爱护水资源是每个公民应尽的责任和义务.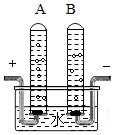 如图是电解水的简易装置图.试回答下列问题:
如图是电解水的简易装置图.试回答下列问题: