题目内容
12.现有一包白色固体可能含有CaO、CuSO4、K2SO4、BaCl2、K2CO3中的一种或几种,为确定其成分,进行如下实验: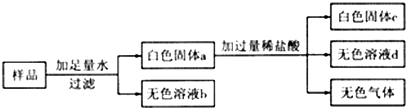
(1)上述实验过程中,产生的无色气体是二氧化碳;
(2)原白色固体中可能有CaO,检验是否有CaO的操作是:取少量无色溶液b.于试管中,加入足量的氯化钙溶液,滴加酚酞试液.经检验原白色固体中确实不含有CaO.
(3)综合分析以上实验,可知原白色固体的成分是硫酸钾、氯化钡和碳酸钾.
(4)下列设想合理的是AB.
A.用白色固体a除去氯化钡中少量的盐酸
B.用无色溶液d鉴别氢氧化钠溶液和碳酸钠溶液.
分析 考虑碳酸钡和稀硝酸反应生成硝酸钡、水和二氧化碳;
硫酸铜溶液是蓝色的,氧化钙和水反应生成氢氧化钙;
硫酸钾和氯化钡反应生成硫酸钡沉淀和氯化钾,碳酸钾和氯化钡反应生成碳酸钡沉淀和氯化钾;
硫酸钡不能和稀盐酸反应,碳酸钡和稀盐酸反应生成氯化钡、水和二氧化碳.
解答 解:硫酸铜溶液是蓝色的,氧化钙和水反应生成氢氧化钙;
硫酸钾和氯化钡反应生成硫酸钡沉淀和氯化钾,碳酸钾和氯化钡反应生成碳酸钡沉淀和氯化钾;
硫酸钡不能和稀盐酸反应,碳酸钡和稀盐酸反应生成氯化钡、水和二氧化碳;
向样品中加入足量水后,得到无色溶液,说明样品中不含有硫酸铜,加入过量稀盐酸后,仍然含有白色沉淀,说明沉淀c是硫酸钡,进一步说明样品中含有硫酸钾和氯化钡,得到的无色气体是二氧化碳,说明沉淀中含有碳酸钡,进一步说明样品中含有碳酸钾;
(1)上述实验过程中,产生的无色气体是二氧化碳.故填:二氧化碳.
(2)原白色固体中可能有CaO的操作是:取少量无色溶液b于试管中,滴加酚酞试液,酚酞试液不变色,说明原白色固体中确实不含有CaO.故填:于试管中,加入足量的氯化钙溶液,滴加酚酞试液.
(3)综合分析以上实验,可知原白色固体的成分是:硫酸钾、氯化钡和碳酸钾.
(4)A.白色固体a中含有碳酸钡和硫酸钡,加入到含有少量盐酸的氯化钡溶液中时,其中的碳酸钡能和稀盐酸反应,从而除去稀盐酸,该选项方法合理;
B.无色溶液d中含有稀盐酸,分别滴加到氢氧化钠溶液和碳酸钠溶液中时,能够产生气泡的溶液是碳酸钠溶液,无明显现象的是氢氧化钠溶液,该选项方法合理.
故填:AB.
故答案为:
(1)二氧化碳;(2)于试管中,加入足量的氯化钙溶液,滴加酚酞试液;
(3)硫酸钾、氯化钡和碳酸钾.(4)AB.
点评 本题主要考查物质的性质,只有掌握了各种物质的性质,才能够判断物质之间相互转化时的反应物和生成物,从而可以进行各方面的判断.

| A. | 实验室里常储备的酸:盐酸、硫酸、生石灰 | |
| B. | 可做干燥剂的物质:氢氧化钠溶液、浓硫酸、生石灰 | |
| C. | 腐蚀性的物质:盐酸、石灰水、氢氧化钠 | |
| D. | 易挥发的物质:浓硫酸、浓盐酸、浓氨水 |
| A. | 2H--2个氢分子 | B. | $\stackrel{+2}{Mg}$--+2价的镁元素 | ||
| C. | 2${SO}_{4}^{2-}$--2个硫酸根离子 | D. | NO2--二氧化氮 |
| A. | 推进太阳能的开发 | B. | 鼓励多开私家车出行 | ||
| C. | 倡导用煤火力发电 | D. | 支持焚烧农作物秸秆 |
| A. | 铁、锌、钙是人体所需的微量元素 | |
| B. | 健康人体胃液的pH范围是0.5~1.9 | |
| C. | 缺乏维生素C会患坏血病,要多吃蔬菜和水果 | |
| D. | 为预防甲状腺肿大,应在食盐中添加大量的碘元素 |
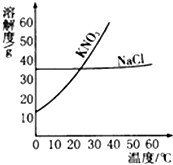 根据如图所示的溶解度曲线,回答下列问题:
根据如图所示的溶解度曲线,回答下列问题: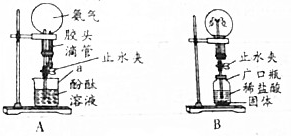 喷泉是一种常见的自然现象,其产生原因是存在较大的压强差.某化学兴趣小组设计了一组“喷泉”实验,两套装置如图所示.
喷泉是一种常见的自然现象,其产生原因是存在较大的压强差.某化学兴趣小组设计了一组“喷泉”实验,两套装置如图所示.