题目内容
3.实验室配制氯化钠溶液的操作中,错误的是( )| A. |  取氯化钠 | B. |  称氯化钠 | C. |  量取水 | D. | 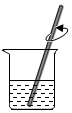 溶解 |
分析 A、根据固体药品的取用方法进行分析判断.
B、根据托盘天平的使用要遵循“左物右码”的原则进行分析判断.
C、根据使用胶头滴管滴加少量液体的方法进行分析判断.
D、根据溶解操作的方法进行分析判断.
解答 解:A、取用固体粉末状药品时,瓶塞应倒放,应用药匙取用,图中所示操作正确.
B、托盘天平的使用要遵循“左物右码”的原则,图中所示操作正确.
C、使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到量筒内或接触量筒内壁,应垂直悬空在量筒口上方滴加液体,防止污染胶头滴管,图中所示操作错误.
D、进行溶解操作时,在烧杯中进行,用玻璃棒进行搅拌,图中所示操作正确.
故选:C.
点评 本题难度不大,熟悉配制一定溶质质量分数溶液的实验步骤、常见化学实验基本操作的注意事项是解答本题的关键.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
11.如图1A~F是实验室制备某些常见气体的装置示意图.

(1)装置图中仪器a的名称为水槽.
(2)用氯酸钾和二氧化锰混合共热制取氧气,写出反应的化学方程式:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)实验室利用B装置制取二氧化碳的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,
如果利用G装置收集二氧化碳,气体应从b 端通入(填“b”或“c”),用C装置代替B装置作为发生装置,其主要优点是可控制反应速率.
(4)排水法收集与排空气法收集CO2的比较(分别用体积相同的2个集气瓶收集)
(5)查阅资料可知:在金属活动性顺序里,位于氢后面的金属Cu,在常温下虽然不能与稀盐酸、稀硫酸反应,但可以与无色硝酸溶液反应,其化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O.
反应生成的NO2是红棕色、有刺激性气味的有毒气体.可用图2所示装置进行实验,请回答:
①检查装置的气密性:关闭弹簧夹,将干燥管放入带有水的烧杯中,若观察到若干燥管内的液(水)面比烧杯内的液(水)面低,且过一段时间后干燥管内的液(水)面保持不变,则表明该装置的
气密性良好.
②打开弹簧夹,用注射器慢慢抽取干燥管内的气体,浓硝酸沿着干燥管慢慢上升,直到硝酸与铜片接触,停止抽拉注射器,关闭弹簧夹,观察干燥管内的现象是:干燥管内出现红棕色气体,铜片表面有气泡产生,铜片溶解,溶液由无色变成蓝色,干燥管内液面下降,反应停止.
③上述实验完成后,须用足量NaOH溶液将气体吸收,其目的是除去二氧化氮气体,防止污染环境.

(1)装置图中仪器a的名称为水槽.
(2)用氯酸钾和二氧化锰混合共热制取氧气,写出反应的化学方程式:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)实验室利用B装置制取二氧化碳的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,
如果利用G装置收集二氧化碳,气体应从b 端通入(填“b”或“c”),用C装置代替B装置作为发生装置,其主要优点是可控制反应速率.
(4)排水法收集与排空气法收集CO2的比较(分别用体积相同的2个集气瓶收集)
| 比较项目 | 排水法 | 向上排空气法 |
收集方法可行性分析 | 因为CO2气体生成和从水面逸出的速率远大于其溶解和与水反应的速率,所以可用排水法收集. | 因为二氧化碳的密度比空气大,所以可用向上排空气法收集. |
收集过程分析 | 用排水法收集CO2,集满现象是: 集气瓶口有大气泡冒出 | “验满”分析:因气体无色,故集满与否较难确定.即便用燃着木条移近容器口火焰熄灭,也难以证明空气完全排尽 |
| 向收集到CO2的集气瓶内倒入等体积适量澄清石灰水,并振荡 | 先浑浊后变澄清所需时间较短 | 先浑浊后变澄清所需时间较长 |
由上述实验可得结论 | 与排空气法相比,排水法的优点是: 用排水法收集的二氧化碳更纯净,现象更明显 | |
反应生成的NO2是红棕色、有刺激性气味的有毒气体.可用图2所示装置进行实验,请回答:
①检查装置的气密性:关闭弹簧夹,将干燥管放入带有水的烧杯中,若观察到若干燥管内的液(水)面比烧杯内的液(水)面低,且过一段时间后干燥管内的液(水)面保持不变,则表明该装置的
气密性良好.
②打开弹簧夹,用注射器慢慢抽取干燥管内的气体,浓硝酸沿着干燥管慢慢上升,直到硝酸与铜片接触,停止抽拉注射器,关闭弹簧夹,观察干燥管内的现象是:干燥管内出现红棕色气体,铜片表面有气泡产生,铜片溶解,溶液由无色变成蓝色,干燥管内液面下降,反应停止.
③上述实验完成后,须用足量NaOH溶液将气体吸收,其目的是除去二氧化氮气体,防止污染环境.
18.下列说法中正确的是( )
| A. | 在蛋白质溶液中加入饱和硫酸铵溶液有沉淀析出 | |
| B. | “加铁酱油”中的“铁”指的是离子 | |
| C. | 通常把pH<7的降水称为酸雨 | |
| D. | 尿素〔CO(NH2)2〕及碳酸氢铵都是有机物 |
8.下列实验方案不合理的是( )
| A. | 用浓氨水、酚酞试液、水及烧杯检验微粒在不断运动 | |
| B. | 用植物的花瓣制作指示剂,检验溶液的酸碱性 | |
| C. | 用氯化钡溶液鉴别硝酸银和硫酸钠两种溶液 | |
| D. | 用燃烧的木条伸入集气瓶中检验CO2是否集满 |
15.除去下列各物质中混有的少量杂质(括号内为杂质),下列方法中,正确的是( )
| A. | 铁粉(C)--加入过量的稀硫酸,过滤 | |
| B. | CO2(H2O)--通过足量的碱石灰,干燥 | |
| C. | NaCl溶液(Na2SO4)--加入过量的Ba(NO3)2溶液,过滤 | |
| D. | CaCl2溶液(HCl)--加入过量的碳酸钙粉末,过滤 |
12.除去物质中的少量杂质,下列所选试剂及操作都正确的是( )
| 序号 | 物质 | 杂质 | 试剂 | 操作 |
| A | CO2 | CO | O2 | 点燃 |
| B | H2 | 水蒸气 | 浓硫酸 | 洗气 |
| C | NaHCO3 | NaCl | 稀盐酸 | 结晶 |
| D | Cu(NO3)2溶液 | CuCl2溶液 | - | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
9.几年前,一辆载满20t电石的挂车,在浙江滨江区燃起熊熊大火并伴有大量黑烟.事故路面上洒落了五六百米燃着的石头.这辆货车在雨中整整燃烧了一天,消防官兵对大火也束手无措,场面让人震撼.大家对电石的化学性质产生了浓厚的兴趣,请你一起与他们完成下列探究活动.
[查阅资料]电石的主要成分是碳化钙(CaC2),可以与水反应生成一种可燃性气体及白色固体.常见的可燃性气体中,乙炔(C2H2)燃烧时伴有大量黑烟.
[猜想与假设]
电石与水反应生成的可燃性气体是:氧气、氢气或乙炔(C2H2);电石与水反应生成的白色固体是:氧化钙、氢氧化钙或碳酸钙.大家做出以上推断的理由是质量守恒定律反应前后元素的种类不变.
大家讨论后一致认为该气体不可能是氧气,原因是氧气不具有可燃性,白色固体不可能是氧化钙,原因是(用化学方程式表示)CaO+H2O═Ca(OH)2.
[实验探究]
[反思交流]
载有电石的货车可以在雨中整整燃烧一天而不熄灭,说明电石与水的反应是放热(填“吸热”或“放热”)反应.
[查阅资料]电石的主要成分是碳化钙(CaC2),可以与水反应生成一种可燃性气体及白色固体.常见的可燃性气体中,乙炔(C2H2)燃烧时伴有大量黑烟.
[猜想与假设]
电石与水反应生成的可燃性气体是:氧气、氢气或乙炔(C2H2);电石与水反应生成的白色固体是:氧化钙、氢氧化钙或碳酸钙.大家做出以上推断的理由是质量守恒定律反应前后元素的种类不变.
大家讨论后一致认为该气体不可能是氧气,原因是氧气不具有可燃性,白色固体不可能是氧化钙,原因是(用化学方程式表示)CaO+H2O═Ca(OH)2.
[实验探究]
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取适量电石加水反应,收集生成的气体,验纯后点燃. | 气体燃烧,产生黄色火焰并伴有浓烈黑烟. | 电石与水反应产生的气体是乙炔(或C2H2) |
| (2)取适量反应后生成的固体于试管中,滴加过量稀盐酸. | 固体溶解,没有气泡产生. | 电石与水反应产生的固体不是碳酸钙 |
| (3)取适量反应后生成的固体于试管中加水,向上层清液中滴加2~3滴酚酞. | 溶液变红 | 电石与水反应产生的固体是氢氧化钙 |
载有电石的货车可以在雨中整整燃烧一天而不熄灭,说明电石与水的反应是放热(填“吸热”或“放热”)反应.