题目内容
1.为探究某干燥的绿色固体粉末的元素组成,某小组进行了如图所示的两个实验,请回答: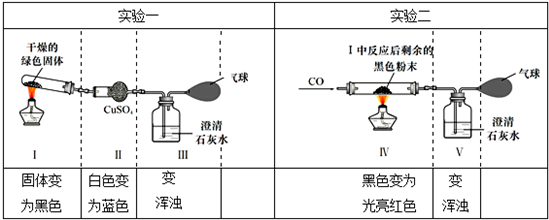
(1)装置Ⅳ中发生反应的化学方程式是CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;
(2)实验二的步骤如下,其正确顺序是:afdcbe;
a、通一段时间的COb、继续通COc、熄灭酒精灯
d、待黑色变成光亮红色e、停止通COf、点燃酒精灯
(3)根据上述实验现象(不考虑溶液中水的挥发)推知绿色固体的元素组成是Cu、C、H、O.
分析 (1)根据黑色粉末的颜色变化来分析;
(2)根据一氧化碳还原氧化铜的实验步骤来分析;
(3)根据质量守恒定律以及实验产物来分析.
解答 解:(1)由实验现象可知,该反应是黑色的氧化铜粉末在加热的条件下被一氧化碳还原成红色的铜,同时生成二氧化碳;故填:CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;
(2)用一氧化碳还原氧化铜时,需要先通入一氧化碳气体,排净装置内的空气(以免加热发生爆炸),后点燃酒精灯加热;反应完成后,先停止加热,再继续通入一氧化碳直到装置冷却(以免温度高的铜被重新氧化);故填:afdcbe;
(3)根据实验现象可知,绿色固体受热分解后生成了水(五水硫酸铜变蓝)、二氧化碳(石灰水变浑浊)和黑色固体,黑色固体与一氧化碳变红色,说明黑色固体为氧化铜,根据质量守恒定律可知,绿色固体粉末中一定含有铜、碳、氧、氢元素;故填:Cu、C、H、O.
点评 解答不同要掌握化学方程式的书写方法和探究实验的设计特点,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
相关题目
15.某同学在实验室配制50g 6%的氯化钠溶液,下列部分操作中错误的是( )
| A. | 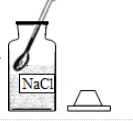 取氯化钠 取氯化钠 | B. |  称氯化钠 称氯化钠 | C. | 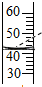 量取水 | D. | 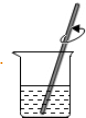 溶解氯化钠 |
9.区别纯净水和过氧化氢溶液最简便的方法是( )
| A. | 滴入澄清石灰水,观察是否浑浊 | |
| B. | 将带火星小木条伸入,观察是否复燃 | |
| C. | 加入MnO2,观察是否产生气泡 | |
| D. | 将燃着的小木条伸入,观察是否更旺 |
 ),它的化学式可写作C2H4O.爆炸时,环氧乙烷先成雾状分散在空气中,然后燃爆,反应的生成物为CO、CO2、H2O.
),它的化学式可写作C2H4O.爆炸时,环氧乙烷先成雾状分散在空气中,然后燃爆,反应的生成物为CO、CO2、H2O.