题目内容
11.硫酸亚铁可用于制颜料、净水剂、防腐剂、消毒剂等.某课外活动小组同学欲利用硫酸厂沸腾炉排出的炉渣(含有Fe2O3、CuO、CuSO4)制取硫酸亚铁并回收铜,主要步骤如图所示.
(1)操作A是过滤;
(2)步骤2中主要发生两个化学反应,其中一个是Fe+Fe2(SO4)3═3Fe SO4,请写出另一个反应的化学方程式;
(3)步骤2中加入过量铁粉的目的是什么?
分析 (1)根据分离混合物的方法来分析;
(2)根据发生的化学反应以及化学方程式的写法来分析;
(3)根据加入铁粉后发生的化学反应以及需要制备的物质来分析.
解答 解:(1)操作A是分离固体与液体的方法,是过滤操作;故填:过滤;
(2)溶液中含有硫酸铜,加入铁粉后,铁与硫酸铜反应生成硫酸亚铁和铜;故填:Fe+CuSO4=FeSO4+Cu;
(3)加入过量的铁粉后,铁能置换出硫酸铜中的铜,同时生成硫酸亚铁;铁能与硫酸铁反应生成硫酸亚铁;故填:置换出硫酸铜中的铜,同时与硫酸铁反应生成硫酸亚铁.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中所给的知识进行解答.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案
相关题目
14.下列能导电的是( )
| A. | 酒精溶液 | B. | 稀硫酸 | C. | 蔗糖溶液 | D. | 氯化钠固体 |
15.下列实验现象描述正确的是( )
| A. | 酚酞滴入稀盐酸中变红 | |
| B. | 红磷燃烧产生白色烟雾 | |
| C. | 研磨氯化铵和熟石灰放出有刺激性气味气体 | |
| D. | 木炭和氧化铜混合物高温加热粉末由红变黑 |
3.20℃时,向200克未知浓度的KNO3溶液中加入10克KNO3后,一定正确的是( )
| A. | 溶液的质量变为210克 | B. | 溶质的质量发生变化 | ||
| C. | 溶质的质量分数变大 | D. | 溶剂的质量不变 |
20.下列四个实验方案设计不合理的是( )
| 选项 | 实验目的 | 方案 |
| A | 鉴别硝酸铵和氯化镁 | 取样,分别与熟石灰混合搅拌,闻气味 |
| B | 鉴别空气和呼出的气体 | 用带火星的木条分别伸入集气瓶中,观察现象 |
| C | 除去CaO中的CaCO3 | 高温加热到固体质量不变 |
| D | 除去CuSO4溶液中的H2SO4 | 加过量氧化铜粉末,过滤 |
| A. | A | B. | B | C. | C | D. | D |
1.晓蜂同学的化学笔记本上有如下记录,你认为不正确的是( )
| A. | 化学反应发生时不一定能观察到明显的现象 | |
| B. | 酸碱中和反应生成盐和水,但是生成盐和水的反应不一定是中和反应 | |
| C. | 书写化学方程式的原则是以客观事实为依据,遵循质量守恒定律 | |
| D. | 一定温度下,向溶液中加入溶质都会使其溶质质量分数增大. |
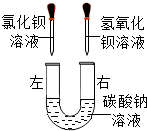 某化学活动小组在一次实验中进行如图所示的实验:
某化学活动小组在一次实验中进行如图所示的实验: