题目内容
8. 某研究性学习小组的同学为探究金属镍(Ni,银白色金属)和铜的活动性顺序,进行了一系列实验活动.请你一起参与他们的活动,并回答有关问题.
某研究性学习小组的同学为探究金属镍(Ni,银白色金属)和铜的活动性顺序,进行了一系列实验活动.请你一起参与他们的活动,并回答有关问题.探究活动一、金属镍和铜的活动性顺序
| 实验方案 | 实验现象 | 实验结论 |
| 将金属镍加入到盛有硫酸铜溶液的试管中 | 溶液的颜色变浅, 有红色固体析出 | 镍比铜的金属活动性强 |
实验过程中,小组同学还发现试管中有无色气体产生的“异常”现象,十分好奇,于是继续进行探究活动.
探究活动二、无色气体的成分是什么?
【猜想假设】A.氢气 B.氧气 C.二氧化硫 D.二氧化碳 E.一氧化碳
【分析推理】小明认为无色气体不可能是二氧化碳或一氧化碳,理由是反应前不含有碳元素.
小红根据二氧化硫能够形成酸雨的事实,推测二氧化硫与二氧化碳的化学性质相似.小组同学认为小红的观点合理,于是将收集到的气体通入石蕊溶液中,发现溶液不变色,证明无色气体不是二氧化硫.
综上所述,小组同学认为,无色气体可能是氢气,或者是氧气.
【设计方案】为确定气体成分,小组同学设计了如下实验方案:
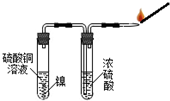
用图所示装置进行实验,先排一会气体,然后将燃着的木条放在尖嘴处,发现气体燃烧并发出淡蓝色火焰,证明无色气体可能是氢气.
该实验方案中浓硫酸的作用是吸水.
【评价与反思】小组同学认为,还可以补充一个实验,验证无色气体中含有氢元素,从而进一步证明无色气体可能是氢气.他们应补充的实验是在火焰上罩一个干而冷的烧杯,杯壁有水雾产生.
分析 根据金属的性质、物质间反应的实验现象、质量守恒定律、浓硫酸的吸水性、氢气燃烧产物的检验进行分析解答即可.
解答 解:将金属镍加入到盛有硫酸铜溶液的试管中,镍比铜的金属活动性强,说明能置换出铜,故会出现红色的固体,故填:红;
镍能与硫酸铜反应生成硫酸镍和铜,故填:Ni+CuSO4=NiSO4+Cu;
因为反应前不含有碳元素,故不可能生成一氧化碳和二氧化碳,故填:反应前不含有碳元素;
二氧化硫能与水反应生成酸,酸能使石蕊试液变色,故可以加入石蕊试液检验是否含有二氧化硫,故填:石蕊;
因为气体具有可燃性,可燃性气体不纯点燃或加热可能产生爆炸,故需要先排一会气体,以使气体纯净,故填:排一会气体;
浓硫酸具有吸水性,能吸收气体带出的水分,故填:吸水;
要验证含有氢元素,因为含有氢元素的物质燃烧会生成水,故可以在燃烧火焰的上方罩一个干而冷的烧杯,观察杯壁有水雾产生,故填:在火焰上罩一个干而冷的烧杯,杯壁有水雾产生.
点评 本题考查的是常见的物质的性质实验探究,完成此题,可以依据已有的知识进行.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
13.下列推论正确的是( )
| A. | 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐 | |
| B. | 酸与碱反应生成盐和水,但生成盐和水的反应不一定是酸与碱的反应 | |
| C. | 若给溶液加水稀释,既可以改变溶液的酸碱度,还可以改变溶液的酸碱性 | |
| D. | 氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物 |
20.为了除去物质中的杂质(括号内物质为杂质),所选用试剂和操作方法都正确的是( )
| 物 质 | 选用试剂 | 操作方法 | |
| A | CO2(HCl) | 过量氢氧化钠溶液 | 通入装有氢氧化钠溶液的洗气瓶 |
| B | NaCl(NH4HCO3) | / | 加热至质量不再减少 |
| C | Cu(NO3)2溶液(AgNO3) | 过量铜粉 | 过滤 |
| D | NaCl溶液(CaCl2) | 过量Na2CO3溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
17.酚酞是一种常用的酸碱指示剂,属于晶体粉末状,几乎不溶于水,其化学式为C20H14O4,下列有关叙述正确的是( )
| A. | 为有机物 | B. | 碳、氢、氧元素质量比为20:14:4 | ||
| C. | 含氧元素质量分数最高 | D. | 该物质是氧化物 |