题目内容
4.氯化钠是一种重要的资源,在海水中储量很丰富.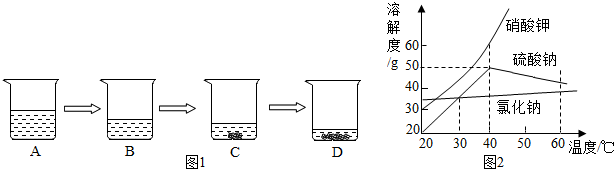
(1)海水晒盐是海水在常温下蒸发得到氯化钠的过程,实验室用氯化钠溶液模拟该过程:
| 物质 | 甲 | 乙 | 丙 |
| 未溶解固体的质量/g | 19 | 5 | 0 |
(2)氯化钠、硝酸钾、硫酸钠的溶解度曲线如图2所示.40℃时,在三个各盛有100g 水的容器中分别加入甲、乙、丙三种纯净物(不含结晶水,不与水反应)各55g,充分溶解后,情况如上表:则物质丙是硝酸钾.
(3)为了除去氯化钠固体中混有的少量硫酸钠杂质,我们可以先把固体放入适量的水中全部溶解,然后进
行下列选项中的操作B(填编号),紧接着再进行操作D(填编号)得到纯净的氯化钠固体.
A.加热蒸发制出现较多固体时,停止加热,利用余热使液体蒸干
B.加热蒸发至剩余少量液体
C.过滤后取滤液
D.过滤后取滤渣.
分析 (1)根据A溶液变化为B溶液,没有晶体析出,BCD都是常温下氯化钠的饱和溶液进行解答;
(2)根据40℃时三种物质的溶解度并结合图示分析解答;
(3)根据氯化钠、硫酸钠的溶解度曲线随温度的变化趋势来分析解答.
解答 解:(1)根据A溶液变化为B溶液,没有晶体析出,所以与B溶液中溶质质量相等的溶液是A;BCD都是常温下氯化钠的饱和溶液,所以与B溶液中溶质质量分数相等的溶液是CD;故填:A;CD;
(2)40℃时硝酸钾的溶解度大于55g,盛有100g 水的容器中加入55g硝酸钾会全部溶解,而氯化钠、硫酸钠,40℃时溶解度小于50g,故物质丙是硝酸钾;
(3)氯化钠的溶解度受温度影响的变化不大,而硫酸钠的溶解度受温度影响的变化较大;故可采取先加热蒸发至剩余少量液体,然后再过滤后取滤渣.
答案:(1)A;CD
(2)硝酸钾
(3)B;D
点评 本题难度比较大,涉及海水晒盐的原理、溶解度曲线应用等理论内容,要通过该题认真总结.

练习册系列答案
相关题目
12.将 50g 98%的浓硫酸全部溶于水配制成 10%的稀硫酸,需要加入水的质量为( )g.
| A. | 400 | B. | 440 | C. | 450 | D. | 500 |
19.下列实验操作、现象与解释对应关系正确的是( )
| 实验操作 | 现象或数据 | 结论 | |
| A. | 向收集满 CO2 的软塑料瓶中加入约 $\frac{1}{3}$ 体积的 NaOH 溶液,旋紧瓶盖,振荡 | 塑料瓶变瘪 | CO2 能与NaOH 反应 |
| B. | 20℃时,将 20gKCl 固体加入 50g 蒸馏水中,充分搅拌溶解后,过滤取滤渣并烘干 | 得到 3g 白色固体 | 20℃时,KCl 的溶解度为 34g |
| C. | 向 20mL 白醋中逐滴加入 10mL 氢氧化钠溶液 | 无明显现象 | 白醋与氢氧化钠不反应 |
| D. | 点燃从导管放出的某气体,在火焰上方罩一个冷而干燥的烧杯 | 烧杯内壁有无色液滴产生 | 该气体是 CH4 |
| A. | A | B. | B | C. | C | D. | D |
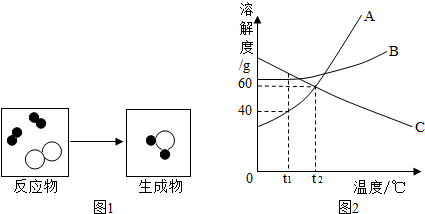
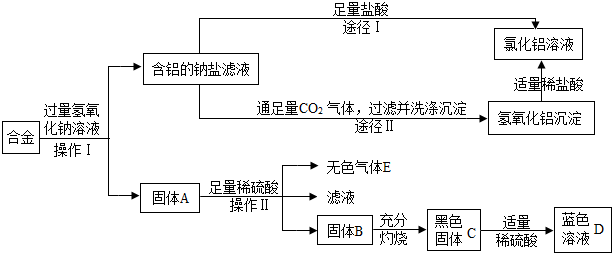
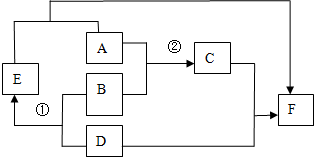
 请写出符合下列条件的化学方程式各一个:
请写出符合下列条件的化学方程式各一个: