题目内容
6.每到冬天,市场上便有一种“热宝”出售,它是一个装有化学药品的小袋.使用时,撕去它的保护膜贴在身体上,不久便会产生热量.已知小袋中装有铁粉、碳粉和少量氯化钠.(1)“热宝”发热的原理是铁粉锈蚀过程中会放出热量.猜测碳粉和氯化钠的作用可能是加快铁粉的锈蚀.
(2)将袋内物质放在足量O2中燃烧,写出反应的化学方程式:
①C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,②3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
(3)使用过后,失效的“热宝”加热盐酸会看到的现象是溶液由无色变成黄色,反应的化学方程式为6HCl+Fe2O3═2FeCl3+3H2O.
分析 (1)根据铁的锈蚀条件以及促进金属锈蚀的方法来分析;
(2)袋内物质碳能燃烧生成二氧化碳,铁燃烧能生成四氧化三铁;
(3)根据反应过程来分析.
解答 解:(1)铁粉在锈蚀过程中会放出热量,氯化钠起到了加快金属锈蚀的作用;故填:铁粉锈蚀过程中会放出热量;加快铁粉的锈蚀;
(2)碳能燃烧生成二氧化碳,铁燃烧能生成四氧化三铁,所以本题答案为:①C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,②3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
(3)失效后的铁粉变成了氧化铁,与稀盐酸反应生成氯化铁和水,看到溶液由无色变成黄色,故填:溶液由无色变成黄色;6HCl+Fe2O3═2FeCl3+3H2O.
点评 本题考查了金属锈蚀及其防护的知识和金属活动性顺序的应用,完成此题,可以依据已有的知识进行.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
16.下列做法正确的是( )
| A. | 处理金属废弃物的方法是填埋法 | |
| B. | 室内放一盆水能防止一氧化碳中毒 | |
| C. | 家用电器着火,立即用水浇灭 | |
| D. | 天然气泄漏,应立即关闭阀门并开窗通风 |
14.将足量的溶质质量分数为20%的盐酸溶液逐渐加入到硫酸钡和碳酸钡组成的100克固体混合物中,直到气体不再产生为止,蒸干后称量所得固体质量为102.2克,则和碳酸钡反应用去的盐酸溶液的质量是( )
| A. | 5.25g | B. | 18.25g | C. | 36.5g | D. | 73g |
1.下列实验不能达到目的是( )
| A. | 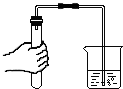 检查气密性 | B. | 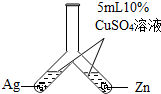 比较金属活动性 | ||
| C. | 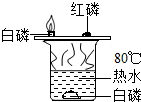 验证燃烧需O2 | D. | 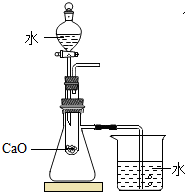 验证反应放热 |