题目内容
3.尿素是氮肥中最主要的一种,其化学式为CO(NH2)2,试计算:(1)尿素的相对分子质量;
(2)尿素中碳元素与氮元素的质量比.
(3)100kg尿素的含氮量与多少千克硫酸铵的含氮量相当.
分析 (1)根据相对分子质量的计算方法计算即可.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:(1)尿素[CO(NH2)2]的相对分子质量是12+16+(14+2)×2=60;
(2)尿素中碳、氮元素的质量比12:(14×2)=3:7.
(3)尿素中氮元素的质量分数是$\frac{14×2}{60}$×100%≈46.7%;
100kg尿素中含氮元素质量为100kg×46.7%=46.7kg;
硫酸铵的相对分子质量:(14+1×4)×2+32+16×4=132.
与100kg尿素的肥效相当的硫酸铵质量为46.7kg÷$\frac{14×2}{132}$≈220kg.
故答案为(1)60;(2)3:7;(3)220kg.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
14.我国科学家屠呦呦因从青蒿中提取可以预防和治疗疟疾的药物青蒿素(C15H22O5)而获得诺贝尔奖.下列关于青蒿素的说法正确着是( )
| A. | 青蒿素是一种有机高分子化合物 | |
| B. | 青蒿素中碳、氧元素个数比为3:1 | |
| C. | 青蒿素中氢元素的质量分数最小 | |
| D. | 青蒿素由15个碳原子、22个氢原子和5个氧原子构成 |
11.人体内的一些液体的pH范围如表,正常情况下,这些液体中一定呈酸性的是( )
| 液体 | 血浆 | 乳汁 | 唾液 | 胆汁 | 胰液 | 胃液 |
| pH范围 | 7.35-7.45 | 6.6-7.6 | 6.6-7.1 | 7.1-7.3 | 7.5-8.0 | 0.9-1.5 |
| A. | 血浆 | B. | 乳汁 | C. | 唾液 | D. | 胃液 |
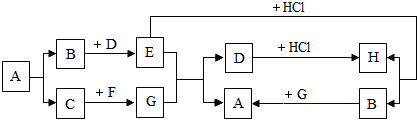
 某学习小组的同学以盖房子的游戏来建立几种重要物质之间的联系,如图,游戏规则是上、下相邻的物质间均可发生反应.
某学习小组的同学以盖房子的游戏来建立几种重要物质之间的联系,如图,游戏规则是上、下相邻的物质间均可发生反应.

 整套茶具中还需要一些辅助器具.
整套茶具中还需要一些辅助器具.