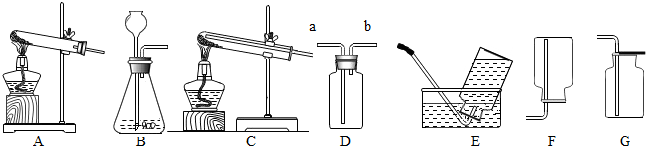
题目内容
16.已知加热浓硫酸和碳能发生下列化学反应:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,其中生成的二氧化硫能使紫色的高锰酸钾溶液褪色,还能使澄清的石灰水变浑浊.某兴趣小组同学为检验该实验的生成物,在老师的指导下设计了如下装置: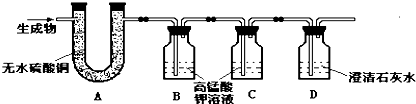
实验时观察到A装置中白色粉末变为蓝色;B装置中紫色溶液褪色,D中澄清石灰变浑浊.针对观察到的现象,他们展开讨论:
小茗同学认为:通过实验能确定反应生成的三种物质H2O、SO2和CO2.
晓骏同学提出:通过实验能确定H2O和SO2我没意见.但SO2和CO2都能使澄清的石灰水变浑浊,会不会是生成的SO2使澄清的石灰水变浑浊?
(1)根据装置A中发生的现象可确定生成了水;
(2)写出SO2使澄清的石灰水变浑浊的化学方程式:Ca(OH)2+SO2═CaSO3↓+H2O.
(3)在一旁的老师给了他们指导,使他俩幡然醒悟.你觉得老师给出了怎样的点拨?C中紫色溶液不褪色,D中澄清石灰水变浑浊.
分析 无水硫酸铜能和水反应生成蓝色五水硫酸铜;
二氧化硫能和氢氧化钙反应生成亚硫酸钙沉淀和水.
解答 解:(1)根据装置A中白色粉末变为蓝色可确定生成了水.
故填:A.
(2)SO2使澄清的石灰水变浑浊,是因为二氧化硫和氢氧化钙反应生成了亚硫酸钙和水,反应的化学方程式为:Ca(OH)2+SO2═CaSO3↓+H2O.
故填:Ca(OH)2+SO2═CaSO3↓+H2O.
(3)因为C中紫色溶液不褪色,D中澄清石灰水变浑浊,说明使澄清石灰水变浑浊的是二氧化碳.
故填:C中紫色溶液不褪色,D中澄清石灰水变浑浊.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
20.下列图象能正确反映其对应的实验操作的是( )
| A. | 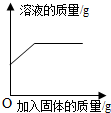 一定温度下,向饱和的硝酸钾溶液中不断加入硝酸钾固体 | |
| B. | 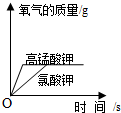 等质量的高锰酸钾和氯酸钾分解制氧气 | |
| C. | 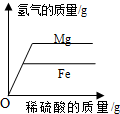 向等质量的镁粉和铁粉中缓慢地逐滴加入稀硫酸 | |
| D. | 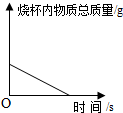 碳酸钠和稀盐酸在烧杯中反应 |
4.为挖掘弘扬临海美食,丰富群众生活,我市在2012中国临海古城文化节活动期间(11月21日至11月25日)将在临海市体育中心西广场(张洋路边)举办临海特色风味美食节.白水洋豆腐是临海美食节上的一道名菜.在豆腐加工时需加入凝固剂,凝固剂的化学成分是什么?通过查资料获悉:凝固剂中可能含有Na2SO4、Ca(OH)2、MgCl2、NaCl等,为验证其成分,小白,小水和小洋进行了如下实验:
(1)根据以上现象,凝固剂溶液中肯定没有Ca(OH)2(或氢氧化钙);
(2)写出实验2中发生的化学反应方程式Ba(N03)2+Na2S04=BaS04↓+2NaN03;
(3)写出实验3中出现的白色沉淀物质的化学式AgCl.
| 实验 | 实验操作 | 实验现象 |
| 1 | 取少量凝固剂溶液于试管中,加入几滴无色酚酞试液 | 仍为无色溶液 |
| 2 | 再取少量凝固剂溶液于试管中,加入适量的Ba(NO3)2溶液和过量稀HNO3 | 有白色沉淀 |
| 3 | 取实验2中的适量滤液于试管中,加入适量的AgNO3溶液和稀HNO3 | 有白色沉淀 |
(2)写出实验2中发生的化学反应方程式Ba(N03)2+Na2S04=BaS04↓+2NaN03;
(3)写出实验3中出现的白色沉淀物质的化学式AgCl.
1.下列是我市2015年基本实验操作考试中的部分考生的操作,其中没有错误的是( )
| A. | 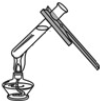 加热液体 | B. |  倾倒液体 | C. |  量取液体 | D. | 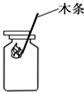 氧气验满 |
6.下列应用和相应的原理(用化学方程式表示)及基本反应类型均正确的是( )
| A. | 铁丝在氧气中燃烧 2Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 化合反应 | |
| B. | 比较铜和银的活动性 Cu+2AgCl═CuCl2+2Ag 置换反应 | |
| C. | 用稀硫酸除铁锈 Fe2O3+2H2SO4═2FeSO4+3H2O 复分解反应 | |
| D. | 除去氧化钙中的碳酸钙 CaCO3$\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑ 分解反应 |