题目内容
12.我国“海洋石油981”钻井平台在西沙开钻,标志着我国能源开发迈上了新台阶.(1)目前,人类使用的燃料大都来自化石燃料,如煤、石油和天然气等,他们都属于不可再生资源(选填再生或不可再生).火让人们从蛮荒走向文明,要想生火必须同时满足的条件有:可燃物、氧气和着火点.生活中发现:点燃的小木棒燃烧端朝上,往往没燃尽就熄灭,而燃烧端朝下,往往不易熄灭.从燃烧的条件来看,你认为燃烧端朝上的小木棒,没燃尽就熄灭的最主要原因是小木棒温度不易达到着火点,若将小木棒事先涂油,燃烧端朝上也不易熄灭,请说明原因.着火点较低的油燃烧产生的热量,使小木棒温度较易达到着火点
(2)“嫦娥三号”探测器于去年12月在西昌卫星发射中心成功发射,承担发射任务的长征乙火箭三子级使用的推进剂是液氢和液氧,液氢在液氧中燃烧的化学反应方程式是:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,该反应的基本类型是化合反应,根据反应方程式提供的信息,可以判断氢气是理想能源的依据是C(填序号.)
A.氢气便于贮藏运输 B.制造氢气的资源丰富
C.氢气燃烧产物不污染空气 D.获得氢气的成本低.
分析 (1)三大化石燃料煤、石油、天然气;
(2)根据化学方程式的书写,氢气的特点进行分析,煤、石油、天然气是化石燃料;氢气燃烧能生成水,属于化合反应;根据其燃烧的产物确定作为燃料的优点,据此解答.
解答 解:(1)目前,人类使用的燃料大都来自化石燃料,如煤、石油和天然气等,他们都属于不可再生资源.火让人们从蛮荒走向文明,要想生火必须同时满足的条件有:可燃物、氧气和着火点.燃烧端朝上的小木棒,热量上升使下端的木条的温度达不到木头的着火点,所以没燃尽就熄灭;
若将小木棒事先涂油,燃烧端朝上也不易熄灭,是因为着火点较低的油燃烧产生的热量,使小木棒温度较易达到着火点,
故答案为:天然气;不可再生;氧气;着火点;小木棒温度不易达到着火点;着火点较低的油燃烧产生的热量,使小木棒温度较易达到着火点
(2)氢气燃烧能生成水,属于化合反应,氢气燃烧的产物是水,不污染空气,是最理想的清洁能源.
故答案为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,化合反应,C.
点评 本题考查三大化石燃烧,氢气所氧气的反应,化学方程式的书写,完成此题,可以依据已有的知识进行.

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
2.实验室用双氧水制氧气和大理石与盐酸反应制二氧化碳相比较,不正确的是( )
| A. | 反应都不需要加热 | B. | 反应原理都是分解反应 | ||
| C. | 所用药品的状态相同 | D. | 都能用向上排空气法收集 |
20.小组同学查资料知道泡沫灭火器原理是:AlCl3+3NaHCO3=3NaCl+Al(OH)3↓+3CO2↑
【提出问题】此反应发生的原因是否由于AlCl3呈酸性?
【实验】测定AlCl3溶液的酸碱性
(1)用紫色石蕊试液测定溶液的酸碱性.
【提出问题】NH4Cl溶液呈酸性,它是否也能与NaHCO3溶液反应?
【实验】按如图进行实验:
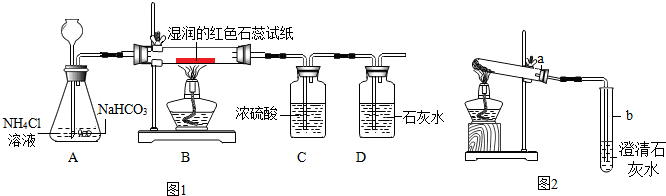
观察到的现象是:湿润的红色石蕊试纸变蓝,石灰水变浑浊
(2)说明生成的气体有NH3和CO2.
(3)C中浓硫酸吸收水蒸气和氨气
(4)A中的反应方程式是NaHCO3+NH4Cl=NaCl+NH3↑+CO2↑+H2O.
【实验反思】Ⅰ、Na2CO3和 NaHCO3的性质区别
按图2进行实验:取适量的NaHCO3粉末加到a试管中,加热,观察到a试管口有水生成,b试管中澄清石灰水变浑浊.持续加热直至两试管均不再发生变化时,发现a试管中仍残留有较多白色固体粉末.
(5)小文猜测白色固体粉末可能是:①NaOH;②Na2CO3;③NaCl.小燕认为猜想③一定不正确,理由是小苏打中不含氯元素,小燕从试管内取少量白色固体溶于水,滴加酚酞,溶液变红,她判断该固体为NaOH,小美认为她的实验设计不合理,因为碳酸钠溶液也可以使酚酞变红.
(6)他们继续探究固体成分,设计了如下实验:
通过实验证明:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$ Na2CO3+CO2↑+H2O,NaHCO3热稳定性较Na2CO3差.
【提出问题】此反应发生的原因是否由于AlCl3呈酸性?
【实验】测定AlCl3溶液的酸碱性
(1)用紫色石蕊试液测定溶液的酸碱性.
【提出问题】NH4Cl溶液呈酸性,它是否也能与NaHCO3溶液反应?
【实验】按如图进行实验:

观察到的现象是:湿润的红色石蕊试纸变蓝,石灰水变浑浊
(2)说明生成的气体有NH3和CO2.
(3)C中浓硫酸吸收水蒸气和氨气
(4)A中的反应方程式是NaHCO3+NH4Cl=NaCl+NH3↑+CO2↑+H2O.
【实验反思】Ⅰ、Na2CO3和 NaHCO3的性质区别
按图2进行实验:取适量的NaHCO3粉末加到a试管中,加热,观察到a试管口有水生成,b试管中澄清石灰水变浑浊.持续加热直至两试管均不再发生变化时,发现a试管中仍残留有较多白色固体粉末.
(5)小文猜测白色固体粉末可能是:①NaOH;②Na2CO3;③NaCl.小燕认为猜想③一定不正确,理由是小苏打中不含氯元素,小燕从试管内取少量白色固体溶于水,滴加酚酞,溶液变红,她判断该固体为NaOH,小美认为她的实验设计不合理,因为碳酸钠溶液也可以使酚酞变红.
(6)他们继续探究固体成分,设计了如下实验:
| 操作步骤 | 实验现象 | 结论 |
| 取少量白色固体于试管中,加水溶解,向其中滴加足量氯化钙溶液 | 出现白色沉淀 | 剩余的固体有Na2CO3 |
| 静置,继续滴加酚酞 | 不变红 | 剩余的固体没有NaOH |
7.下列气体,属于纯净物是( )
| A. | 洁净的空气 | B. | 汽车尾气 | C. | 水蒸气 | D. | 石灰石 |
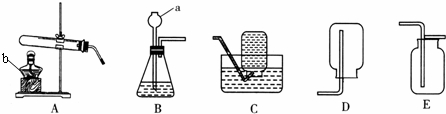
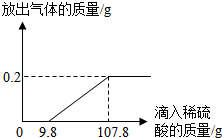 在烧杯中加入2.14g久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示.请回答下列问题:
在烧杯中加入2.14g久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示.请回答下列问题: