题目内容
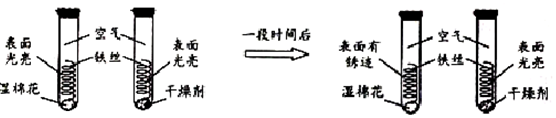
19.铝、铜、铁是生活中常见的金属.(1)铁制品锈蚀,实际上是铁跟空气中的氧气和水发生了化学反应.防止铁制栏杆锈蚀的一种方法是刷漆.
(2)为探究这三种金属的活动性强弱顺序,小明将打磨过的铁丝、铝丝分别放入稀硫酸,通过观察他得出:铝的活动性比铁强.他得出该结论的依据是铝丝与稀硫酸反应产生气泡的速率比铁快.要验证三种金属的活动性强弱顺序,还需补做一个实验将打磨过的铜丝插入稀硫酸中.
分析 (1)根据铁的锈蚀条件以及防锈措施来分析;
(2)探究三种金属的活动性强弱顺序,根据反应的快慢和是否与酸反应.
解答 解:(1)铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果.根据防止铁制品生锈的常用措施可知,防止铁制栏杆锈蚀的一种方法是:刷漆;故填:氧气;水;刷漆;
(2)铝丝与稀硫酸反应快,推测金属活动性:铝>铁,补充铜丝插入稀硫酸中,观察是否反应,故能得出活动性Al>Fe>H>Cu的结论.
故答案为:铝丝与稀硫酸反应产生气泡的速率比铁快;将打磨过的铜丝插入稀硫酸中.
点评 本题考查学生对金属的性质及金属锈蚀的条件及其防护措施的理解与在解题、生活中应用的能力.

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
9.某兴趣小组同学对实验室制备氧气的催化剂进行如下探究.
【提出问题】
①二氧化锰常作为氯酸钾分解制取氧气的催化剂,那其他氧化物是否也能催化氯酸钾分解呢?是否比二氧化锰催化效果更好?
【查阅资料】
研究表明,许多金属氧化物对氯酸钾的分解(分解时放出热量)有催化作用.分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如表所示:
实验室用氯酸钾制取氧气,如果不用二氧化锰作催化剂,最好选用的氧化物是氧化铜.
【设计并完成实验】
Ⅰ.将3.0g氯酸钾放在试管中加热
Ⅱ.将3.0g氯酸钾与1.0g二氧化锰混合均匀加热
Ⅲ.将Xg氯酸钾与1.0g氧化铜混合均匀加热
【实验现象分析】
将实验Ⅲ反应后的固体加水溶液、过滤、洗涤、干燥,若称量得到1.0g黑色粉末,再将黑色粉末和Xg氯酸钾混合加热,现象与实验Ⅲ相同.Ⅲ中X的值应为3.0,实验I和Ⅲ比较可证明CuO改变KClO3分解的速率.
【结论】
氧化铜也能做氯酸钾分解的催化剂,实验Ⅲ中的化学反应方程式为2KClO3$\frac{\underline{\;CuO\;}}{△}$2KCl+3O2↑.
(注意:若答对该题奖励4分,化学十九总分不超过60分)
【实验反思】
(1)实验Ⅱ和Ⅲ对比的目的是CuO对KClO3催化效果是否比MnO2好.
(2)在相同温度下比较两组实验产生氧气的快慢,通常可采用的方法有:
①测量相同时间内收集氧气的体积大小;
②测量收集相同体积氧气所需要时间长短.
【提出问题】
①二氧化锰常作为氯酸钾分解制取氧气的催化剂,那其他氧化物是否也能催化氯酸钾分解呢?是否比二氧化锰催化效果更好?
【查阅资料】
研究表明,许多金属氧化物对氯酸钾的分解(分解时放出热量)有催化作用.分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如表所示:
| 氧化铁 | 氧化铝 | 氧化铜 | 氧化镁 | |
| 开始反应 | 420 | 515 | 305 | 490 |
| 剧烈反应 | 490 | 540 | 350 | 545 |
【设计并完成实验】
Ⅰ.将3.0g氯酸钾放在试管中加热
Ⅱ.将3.0g氯酸钾与1.0g二氧化锰混合均匀加热
Ⅲ.将Xg氯酸钾与1.0g氧化铜混合均匀加热
【实验现象分析】
将实验Ⅲ反应后的固体加水溶液、过滤、洗涤、干燥,若称量得到1.0g黑色粉末,再将黑色粉末和Xg氯酸钾混合加热,现象与实验Ⅲ相同.Ⅲ中X的值应为3.0,实验I和Ⅲ比较可证明CuO改变KClO3分解的速率.
【结论】
氧化铜也能做氯酸钾分解的催化剂,实验Ⅲ中的化学反应方程式为2KClO3$\frac{\underline{\;CuO\;}}{△}$2KCl+3O2↑.
(注意:若答对该题奖励4分,化学十九总分不超过60分)
【实验反思】
(1)实验Ⅱ和Ⅲ对比的目的是CuO对KClO3催化效果是否比MnO2好.
(2)在相同温度下比较两组实验产生氧气的快慢,通常可采用的方法有:
①测量相同时间内收集氧气的体积大小;
②测量收集相同体积氧气所需要时间长短.
10.下列关于溶解度的说法正确的是( )
| A. | 100克水最多可溶解36克氯化钠,则氯化钠的溶解度为36克 | |
| B. | 20℃时100克饱和氯化钠溶液中含有26克氯化钠,则20℃时氯化钠的溶解度为26克 | |
| C. | 25℃时100克水中溶解了35克氯化钠,则25℃时氯化钠的溶解度为35克 | |
| D. | 20℃时50克水中最多溶解氯化钠18克,则20℃时氯化钠的溶解度为36克 |
7.美琪同学家新换了水龙头,她从说明书上了解到该水龙头是铜质镀铬材料.出于好奇,美琪想探究铬(Cr)与常见金属铁、铜的活动性强弱,请你一同参与.
【知识回放】
金属活动性顺序:K Ca Na Mg Al ZnFeSn Pb(H)CuHgAg Pt Au,(请你在横线上填写对应金属的元素符号).
【作出猜想】
猜想一:Cr>Fe>Cu
猜想二:Fe>Cu>Cr
猜想三:Fe>Cr>Cu.
【查阅资料】
①铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】
美琪取形状大小相同的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸,将三种金属片分别放入试管中,观察现象.
【结论与解释】
(1)美琪得到的正确结论是猜想一.
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜.
【知识运用】
(1)将铬片投入FeSO4溶液中,反应能(填“能”或“不能”)进行.
(2)写出探究铬、铁、铜的活动性强弱的另外两组试剂:硫酸铬溶液、铁、硫酸铜溶液;铬、铜、硫酸亚铁溶液.(每一组仅限三种试剂)
【知识回放】
金属活动性顺序:K Ca Na Mg Al ZnFeSn Pb(H)CuHgAg Pt Au,(请你在横线上填写对应金属的元素符号).
【作出猜想】
猜想一:Cr>Fe>Cu
猜想二:Fe>Cu>Cr
猜想三:Fe>Cr>Cu.
【查阅资料】
①铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】
美琪取形状大小相同的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸,将三种金属片分别放入试管中,观察现象.
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验操作 |  |  |  |
| 实验现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变为蓝色 | 无明显现象 |
(1)美琪得到的正确结论是猜想一.
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜.
【知识运用】
(1)将铬片投入FeSO4溶液中,反应能(填“能”或“不能”)进行.
(2)写出探究铬、铁、铜的活动性强弱的另外两组试剂:硫酸铬溶液、铁、硫酸铜溶液;铬、铜、硫酸亚铁溶液.(每一组仅限三种试剂)
14. 用某金属颗粒与足量的稀盐酸反应,如生成氢气的质量(以纵坐标表示,单位:g)与所用金属的质量(以横坐标表示,单位:g)之间的关系如图,该金属颗粒可能是( )
用某金属颗粒与足量的稀盐酸反应,如生成氢气的质量(以纵坐标表示,单位:g)与所用金属的质量(以横坐标表示,单位:g)之间的关系如图,该金属颗粒可能是( )
 用某金属颗粒与足量的稀盐酸反应,如生成氢气的质量(以纵坐标表示,单位:g)与所用金属的质量(以横坐标表示,单位:g)之间的关系如图,该金属颗粒可能是( )
用某金属颗粒与足量的稀盐酸反应,如生成氢气的质量(以纵坐标表示,单位:g)与所用金属的质量(以横坐标表示,单位:g)之间的关系如图,该金属颗粒可能是( )| A. | 纯净的锌 | B. | 含铜的锌 | ||
| C. | 含有不与酸反应的杂质的锌 | D. | 含有不与酸反应的杂质的铁 |
11.下列有关溶液的说法中,正确的是( )
| A. | 固体物质的溶解度都随温度的升高而增大 | |
| B. | 一定温度下,饱和溶液增加溶剂一定变为不饱和溶液 | |
| C. | 将30 g硝酸钾投入到70 g水中,所得溶液质量一定是100 g | |
| D. | 5 g食盐完全溶于100 g水中,所得溶液中溶质的质量分数为5% |
 某化学兴趣小组在做Fe和CuSO4溶液反应实验时,发现生成Cu的同时有气泡产生.为了进一步研究做了如下实验:
某化学兴趣小组在做Fe和CuSO4溶液反应实验时,发现生成Cu的同时有气泡产生.为了进一步研究做了如下实验: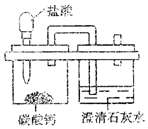 用如图微型仪器完成制取并检验CO2的实验只消耗了0.55g 10%的盐酸.求:
用如图微型仪器完成制取并检验CO2的实验只消耗了0.55g 10%的盐酸.求: