题目内容
13. 新药帕拉韦注射液可用于抑制H7N9禽流感,其说明书部分内容如图:
新药帕拉韦注射液可用于抑制H7N9禽流感,其说明书部分内容如图:(1)帕拉米韦由四种元素组成;
(2)帕拉米韦中氢、氧的原子个数比7:1;
(3)H,N两种元素的质量比为1:2
(4)成人禽流感患者,每天应注射帕拉米韦6支
(5)32.8g的帕拉米韦中氧元素的质量为6.4g.
分析 (1)根据化学式的意义进行分析判断;
(2)根据化合物中各元素原子个数之比,进行分析判断;
(3)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析;
(4)若每支注射液中帕拉米韦的含量为25mg/支,成人用量为75mg/次,2次/日,据此进行分析解答;
(5)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:(1)由帕拉米韦的化学式可知,它是由碳、氢、氧、氮四种元素的;故填:四;
(2)由帕拉米韦的化学式可知,帕拉米韦中氢、氧的原子个数比28:4=7:1;故填:7:1;
(3)帕拉米韦中H、N两种元素的质量比为(1×28):(14×4)=1:2.故填:1:2;
(4)每支注射液中帕拉米韦的含量为25mg/支,成人用量为75mg/次,2次/日,则成人每日需注射量为75mg/次×2次=150mg,则每天应注射帕拉米韦注射液150mg÷25mg/支=6支,故填:6;
(5)32.8g的帕拉米韦中氧元素的质量为32.8g×$\frac{16×4}{12×15+1×28+14x+16×4}×100%$=6.4g;故填:6.4.
点评 本题难度不大,考查同学们结合标签新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
3.地壳中含量最多的金属元素、非金属元素和空气中含量最多的元素组成的化合物的化学式是( )
| A. | AlNO3 | B. | Al2O3 | C. | Al(NO3)3 | D. | Al(OH)3 |
4.下列变化属于物理变化的是( )
| A. | 粮食酿酒 | B. | 干冰升华 | C. | 纸张燃烧 | D. | 铁钉生锈 |
1.下列实验操作中,正确 的是( )
| A. |  取用药品 | B. |  干燥二氧化碳 干燥二氧化碳 | C. |  测定某溶液的pH | D. |  滴加液体 |
8.除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
| 物质 | 杂质 | 除杂所用的试剂和方法 | |
| A | Ca(OH)2固体 | CaCO3固体 | 加入适量的稀盐酸 |
| B | O2气体 | N2气体 | 通过灼热的Cu |
| C | MgCl2溶液 | NaCl溶液 | 先加入过量的NaOH溶液,再过滤 |
| D | H2气体 | HCl气体 | 先通过NaOH溶液,再通过浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
5.工业上以大理石和赤铁矿为主要原料制取建筑材料B和金属G,其转化关系如图所示,已知DG为单质.下列推断不正确的是( )
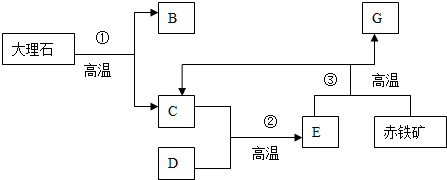

| A. | 些反应流程可降低碳的排放 | B. | G是单质铁 | ||
| C. | ③是置换反应 | D. | 本过程可循环使用的物质是C |
2.下列实验选用的用品一定不需要的是( )
| A. | 碳酸钠溶液pH值测定(玻璃棒) | B. | 粗盐提纯(蒸发皿) | ||
| C. | 蒸馏自来水制蒸馏水(石棉网) | D. | 硝酸钾与食盐的分离(分液漏斗) |
3.下列实验能达到相应目的是( )
| A. | 分离Zn和Cu的固体混合物:适量的Cu(NO3)2溶液,过滤 | |
| B. | 除去CaCl2溶液中少量的HCl:加过量Ca(OH)2固体,过滤 | |
| C. | 验证BaSO4中含有BaCO3:取样,加适量稀盐酸有气泡产生 | |
| D. | 制备Cu(OH)2:将CuSO4溶液和适量Ba(OH)2溶液混合,过滤. |