题目内容
6.按要求填空.(1)用小苏打治疗胃酸过多的化学反应方程式NaHCO3+HCl═NaCl+H2O+CO2↑
(2)用稀硫酸除铁锈的化学反应方程式的化学反应方程式Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
(3)用氢氧化钠溶液吸收煤燃烧产生的二氧化硫气体的化学反应方程式2NaOH+SO2═Na2SO3+H2O
(4)锌与过量稀盐酸反应后溶液溶液中的溶质的化学式ZnCl2
(5)用于消除公路积雪的日常生活用盐的化学式NaCl.
分析 首先根据题意确定物质的化学名称、反应原理,然后根据书写化学式与化学方程式的方法和步骤写出物质的化学式即可.
解答 解:(1)小苏打是碳酸氢钠的俗称,胃酸主要是盐酸,二者反应生成氯化钠、水和二氧化碳,化学方程式为:NaHCO3+HCl═NaCl+H2O+CO2↑;
(2)稀硫酸和氧化铁反应能生成硫酸铁和水.稀硫酸和氧化铁反应的化学方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(3)氢氧化钠和二氧化硫反应的化学方程式为:2NaOH+SO2═Na2SO3+H2O;
(4)锌和稀盐酸反应生成氯化锌,氯化锌是由显+2价的锌元素和显-1价的氯元素组成的,根据化合价原则,其化学式为:ZnCl2;
(5)氯化钠属于盐,可消除公路积雪,其化学式为:NaCl;
故答案为:(1)NaHCO3+HCl═NaCl+H2O+CO2↑;(2)Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;(3)2NaOH+SO2═Na2SO3+H2O;(4)ZnCl2;(5)NaCl;
点评 书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
17.甲同学误把H2O2溶液当作酸与Fe2O3粉末混合,发现有大量气泡产生.他联想到MnO2可作为H2O2分解的催化剂,那么,Fe2O3能否作为H2O2分解的催化剂呢?请你一起参与探究,并填写下列空白.
【猜想】Fe2O3能作为H2O2分解的催化剂.
【实验验证】甲同学依次设计了三个实验:
实验一 取一定量的H2O2溶液于试管中,观察到有极少量气泡产生,伸入带火星的木条,没有复燃.说明H2O2溶液常温下缓慢分解.
实验二 在实验一的试管中加入W g Fe2O3粉末,有大量气泡产生,然后伸入带火星的木条,木条复燃.说明Fe2O3能加快H2O2的分解速率,该反应的符号表达式是H2O2$\stackrel{Fe_{2}O_{3}}{→}$H2O+O2;
实验三 待反应结束后,将试管里的不溶物滤出,并洗涤、干燥、称量,固体质量仍为W g.说明反应前后Fe2O3的质量保持不变;
【实验结论】甲同学认为,Fe2O3粉末可以作为H2O2分解的催化剂.
反思评价】(1)乙同学认为要证明甲同学的结论正确,仅做这三个实验还不充分,需要再补充一个探究实验.探究反应前后Fe2O3的化学性质是否改变(或反应前后Fe2O3是否转化为其他物质).
(2)除MnO2和Fe2O3外,CuO也可以作H2O2分解的催化剂.
【拓展】下表是丙同学探究影响H2O2分解因素时所记录的部分数据,通过对数据分析,你能得出什么结论?相同条件下,MnO2的催化效果比Fe2O3好(或其他条件相同的情况下,H2O2浓度越大,产生氧气的速率越快).
用足量等体积H2O2溶液制取相同体积O2所需的时间:
【猜想】Fe2O3能作为H2O2分解的催化剂.
【实验验证】甲同学依次设计了三个实验:
实验一 取一定量的H2O2溶液于试管中,观察到有极少量气泡产生,伸入带火星的木条,没有复燃.说明H2O2溶液常温下缓慢分解.
实验二 在实验一的试管中加入W g Fe2O3粉末,有大量气泡产生,然后伸入带火星的木条,木条复燃.说明Fe2O3能加快H2O2的分解速率,该反应的符号表达式是H2O2$\stackrel{Fe_{2}O_{3}}{→}$H2O+O2;
实验三 待反应结束后,将试管里的不溶物滤出,并洗涤、干燥、称量,固体质量仍为W g.说明反应前后Fe2O3的质量保持不变;
【实验结论】甲同学认为,Fe2O3粉末可以作为H2O2分解的催化剂.
反思评价】(1)乙同学认为要证明甲同学的结论正确,仅做这三个实验还不充分,需要再补充一个探究实验.探究反应前后Fe2O3的化学性质是否改变(或反应前后Fe2O3是否转化为其他物质).
(2)除MnO2和Fe2O3外,CuO也可以作H2O2分解的催化剂.
【拓展】下表是丙同学探究影响H2O2分解因素时所记录的部分数据,通过对数据分析,你能得出什么结论?相同条件下,MnO2的催化效果比Fe2O3好(或其他条件相同的情况下,H2O2浓度越大,产生氧气的速率越快).
用足量等体积H2O2溶液制取相同体积O2所需的时间:
| 时间(min) 浓度 催化剂 | 30%H2O2溶液 | 15%H2O2溶液 | 5%H2O2溶液 |
| 加入W g MnO2 | 0.2 | 0.8 | 2.0 |
| 加入W g Fe2O3 | 7.0 | 9.0 | 16.0 |
14.测定生活中一些物质的pH,结果如图.下列说法错误的是( )


| A. | 食醋可以用于去除水垢 | |
| B. | 草木灰与铵态氮肥不能混合使用 | |
| C. | 清洁剂的水溶液能使紫色石蕊试液变红 | |
| D. | 胃酸过多的人不宜多吃柠檬 |
1. 一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程
一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程
度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的BaCl2 溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4 溶液,产生蓝色絮状沉淀.根据实验现象,可确定该固体是NaOH和Na2CO3的混合物;
(2)称取10.6g 该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如下表:
计算该样品中Na2CO3的质量分数50%.
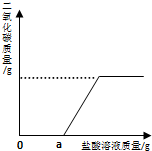
(3)再取固体样品溶于水,加入一定质量分数的稀盐酸,直至过量.测出加入稀盐酸的质量与产生CO2气体的
质量关系如图所示.从图中可以判断:在该样品溶液中加入稀盐酸,首先与之反应的物质是NaOH.
(4)请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀盐酸反应,变质前消耗盐酸的量等于变质后消耗盐酸的量(填“大于”、“小于”或“等于”).
 一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程
一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的BaCl2 溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4 溶液,产生蓝色絮状沉淀.根据实验现象,可确定该固体是NaOH和Na2CO3的混合物;
(2)称取10.6g 该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如下表:
| 样品质量 | 反应前总质量 | 反应后总质量 |
| 10.6克 | 148.5克 | 146.3克 |
(3)再取固体样品溶于水,加入一定质量分数的稀盐酸,直至过量.测出加入稀盐酸的质量与产生CO2气体的
质量关系如图所示.从图中可以判断:在该样品溶液中加入稀盐酸,首先与之反应的物质是NaOH.
(4)请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀盐酸反应,变质前消耗盐酸的量等于变质后消耗盐酸的量(填“大于”、“小于”或“等于”).
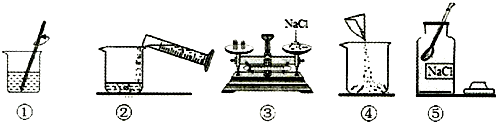
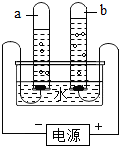 水是常见的物质之一,根据电解水的现象回答下列问题:
水是常见的物质之一,根据电解水的现象回答下列问题: