题目内容
12.镁合金的强度高、机械性能好.这些特性使金属镁成为制造汽车、飞机、火箭的重要材料,从而获得“国防金属”的美誉.海水提镁是国际上的主要趋势,工业流程图如下;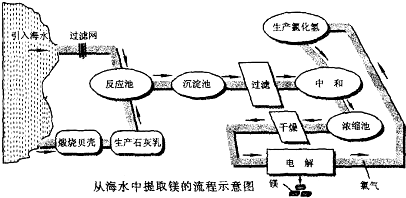
其步骤为:
I.将海边大量存在的贝壳(主要成分为CaCO3)煅烧成生石灰,并将生石灰制成石灰乳
Ⅱ.将石灰乳加入到海水反应池中,经过沉降、过滤得到Mg(OH)2沉淀
Ⅲ.在Mg(OH)2沉淀中加入盐酸中和得到MgCl2溶液,再经蒸发结晶得到MgCl2•6H2O
Ⅳ.将MgCl2•6H2O在一定条件下加热得到无水MgCl2
V.电解熔融的无水MgCl2可得到Mg
(1)请根据上述步骤回答问题:
①写出步骤I、Ⅲ的有关化学方程式:
I.贝壳煅烧成生石灰CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
Ⅲ.Mg(OH)2沉淀中加入盐酸中和Mg(OH)2+2HCl=MgCl2+2H2O.
②步骤I~V中有分解反应的是(填写步骤序号):I、Ⅳ、V.
③上述海水提镁的流程中,采取了循环、回收利用的物质是:氯气. 该设计的优点是降低成本、减少污染.
分析 (1)根据反应物和生成物及其质量守恒定律可以书写化学方程式;
(2)根据分解反应的概念分析即可;
(3)根据工艺流程图来分析.
解答 解:(1)贝壳的主要成分是碳酸钙,锻烧碳酸钙的原理是:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;故填:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;
在Mg(OH)2沉淀中加入盐酸中和得到MgCl2溶液,故填:Mg(OH)2+2HCl=MgCl2+2H2O;
(2)分解反应的概念:由一种物质生成两种或两种以上的物质的反应,I、Ⅳ、V所涉及到的方程式分别为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ MgCl2.6H2O$\frac{\underline{\;\;△\;\;}}{\;}$MgCl2+6H2O MgCl2$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑;故填:I、Ⅳ、V;
(3)电解产生的Cl2用于制取HCl气体,实现盐酸循环利用,减少了环境污染.故填:氯气.
点评 本题以从海水中提取镁为背景,考查物质的分离、提纯,节能减排等知识,培养了学生运用知识的能力.

练习册系列答案
相关题目
2.下列物质均需密封保存,其中既利用了它的物理性质又利用了它的化学性质的是( )
| A. | 生石灰 | B. | 浓硫酸 | C. | 浓盐酸 | D. | 烧碱 |
3.下列不属于氧气的用途的是( )
| A. | 急救病人 | B. | 供航天员呼吸 | C. | 灯泡中充气 | D. | 气焊气割 |
20.化学反应前后,下列各项①原子总数 ②分子总数 ③物质总质量 ④物质的种类 ⑤元素的种类 ⑥原子的种类,一定发生变化的是( )
| A. | ④ | B. | ②④ | C. | ①③⑤ | D. | ①②⑤ |
7.钢铁是使用最多的金属材料.在今年的化学活动周中,某校兴趣小组的同学在老师指导下做了三个有关铁的实验.
实验一:用干燥纯净的一氧化碳还原氧化铁 (实验装置如图1):
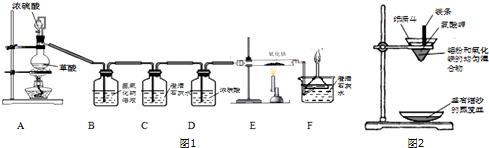
其中A是实验室用草酸(H2C2O4)和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:H2C2O4$\frac{\underline{\;浓硫酸\;}}{加热}$H2O+CO2↑+CO↑.请回答下列问题:
(1)B装置中发生反应的化学方程式是2NaOH+CO2=Na2CO3+H2O.
(2)C装置无明显现象,C装置的作用是证明二氧化碳已被完全吸收.D装置中浓硫酸的作用是干燥一氧化碳气体.
(3)E装置中的实验现象是红色粉末变成黑色.
(4)F装置的作用是证明反应生成了二氧化碳、尾气处理.
实验二:铝粉和氧化铁粉末反应(铝热反应)(实验装置如图2):
图中纸漏斗由两张滤纸折叠成漏斗状套在一起,使四周都有四层,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中.实验后老师作了如下提示:实验中镁条和氯酸钾的作用是提供反应所需的高温条件,铝粉和氧化铁粉末在高温条件下的反应叫铝热反应,属于置换反应,该反应常用于焊接钢轨.请写出该反应的化学方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.该反应中单质铝与一氧化碳有相似的还原(填“氧化”或“还原”)性.
实验后同学们对金属与金属氧化物间的反应产生兴趣,激发了探究热情.
【提出问题】任何金属与金属氧化物在高温条件下都能反应吗?
同学们在请教老师后设计了如下实验方案并进行了探究.
【实验方案】
【实验总结】金属与金属氧化物在高温条件下有些能反应,有些不能反应.
实验三:甲、乙、丙三位同学,分别用上述实验一所得的铁样品与稀硫酸反应,其中只有一位同学所取用
的稀硫酸与铁样品恰好完全反应,实验数据如下表:
请你认真分析数据,回答下列问题:(烧杯的质量为28.1g,计算结果保留一位小数)
(1)乙同学所取用的稀硫酸与铁样品恰好完全反应?
(2)计算样品中铁的质量分数?
(3)计算恰好完全反应后所得溶液中溶质的质量分数?
实验一:用干燥纯净的一氧化碳还原氧化铁 (实验装置如图1):

其中A是实验室用草酸(H2C2O4)和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:H2C2O4$\frac{\underline{\;浓硫酸\;}}{加热}$H2O+CO2↑+CO↑.请回答下列问题:
(1)B装置中发生反应的化学方程式是2NaOH+CO2=Na2CO3+H2O.
(2)C装置无明显现象,C装置的作用是证明二氧化碳已被完全吸收.D装置中浓硫酸的作用是干燥一氧化碳气体.
(3)E装置中的实验现象是红色粉末变成黑色.
(4)F装置的作用是证明反应生成了二氧化碳、尾气处理.
实验二:铝粉和氧化铁粉末反应(铝热反应)(实验装置如图2):
图中纸漏斗由两张滤纸折叠成漏斗状套在一起,使四周都有四层,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中.实验后老师作了如下提示:实验中镁条和氯酸钾的作用是提供反应所需的高温条件,铝粉和氧化铁粉末在高温条件下的反应叫铝热反应,属于置换反应,该反应常用于焊接钢轨.请写出该反应的化学方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.该反应中单质铝与一氧化碳有相似的还原(填“氧化”或“还原”)性.
实验后同学们对金属与金属氧化物间的反应产生兴趣,激发了探究热情.
【提出问题】任何金属与金属氧化物在高温条件下都能反应吗?
同学们在请教老师后设计了如下实验方案并进行了探究.
【实验方案】
| 实验组别 | 实验操作 | 实验现象 | 结论 |
| 实验1 | 取Zn、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 黑色粉末变成红色 固体部分溶解,有气泡产生,水溶液呈无色. | Zn和CuO能发生置换反应. |
| 实验2 | 取Mg、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 发生爆炸,黑色粉末变成红色. 固体部分溶解,有气泡产生,水溶液呈无色. | 镁与氧化铜发生了置换反应 |
| 实验3 | 取Cu、Fe2O3粉末的均匀混合物于密闭容器中,高温加热. | 粉末无变化 | Cu、Fe2O3不能反应. |
实验三:甲、乙、丙三位同学,分别用上述实验一所得的铁样品与稀硫酸反应,其中只有一位同学所取用
的稀硫酸与铁样品恰好完全反应,实验数据如下表:
| 甲 | 乙 | 丙 | |
| 烧杯+稀硫酸 | 200g | 150g | 150g |
| 加入的铁样品 | 9g | 9g | 14g |
| 烧杯+剩余物质质量 | 208.7g | 158.7g | 163.7g |
(1)乙同学所取用的稀硫酸与铁样品恰好完全反应?
(2)计算样品中铁的质量分数?
(3)计算恰好完全反应后所得溶液中溶质的质量分数?
4.我国古代的灿烂文化中与化学无关的是( )
| A. | 烧制陶瓷 | B. | 发明指南针 | C. | 使用火药 | D. | 冶炼钢铁 |
4.下列反应属于分解反应的是( )
| A. | 水 $\stackrel{通电}{→}$ 氧气+氢气 | B. | 铁+氧气 $\stackrel{点燃}{→}$四氧化三铁 | ||
| C. | 红磷+氧气$\stackrel{点燃}{→}$五氧化二磷 | D. | 石蜡+氧气 $\stackrel{点燃}{→}$二氧化碳+水 |
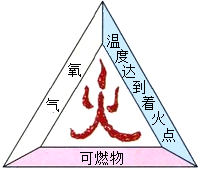 燃烧与我们的生活与社会的发展有着密切的联系.
燃烧与我们的生活与社会的发展有着密切的联系.