题目内容
14.实验室里制取CO2的药品是大理石或石灰石与稀盐酸,化学反应方程式为CaCO3+2HCl═CaCl2+CO2↑+H2O;收集CO2的方法是向上排空气法;检验CO2的方法是将产生的气体通入澄清的石灰水中,澄清的石灰水变浑浊,则证明产生的气体是二氧化碳;验满CO2的方法是将燃着的木条放到集气瓶,若木条熄灭,则证明已满.分析 制取装置包括加热和不需加热两种,实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳;二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了.
解答 解:实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳;二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;故答案为:大理石或石灰石与稀盐酸;CaCO3+2HCl═CaCl2+CO2↑+H2O;向上排空气法;将产生的气体通入澄清的石灰水中,澄清的石灰水变浑浊,则证明产生的气体是二氧化碳;将燃着的木条放到集气瓶,若木条熄灭,则证明已满.
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、检验方法和验满方法等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
9.下列关于氧气物理性质的叙述中,正确的是( )
| A. | 液态氧是没有颜色的 | |
| B. | 氧气难溶于水 | |
| C. | 氧气的密度略小于空气 | |
| D. | 在通常状况下,氧气是没有颜色,没有气味的气体 |
19.有A和B两种物质,在一定条件下反应生成C和D,已知2g A能跟5g B恰好完全反应生成4g C和3g D,现有6g A和20g B,经充分反应后,下列说法中正确的是( )
| A. | 生成C和D的质量之和为26 g | B. | 生成12 g C | ||
| C. | 有1 g A剩余 | D. | 生成10 g D |
4.现有:火柴、一张干燥的白纸、一只洁净干燥的小烧杯、澄清的石灰水,设计一个实验证明纸张燃烧后有水和二氧化碳生成.
| 实验步骤 | 实验现象 | 结论 |
| 点燃纸张,在火焰上方罩上一个冷而干燥的烧杯 | 烧杯内壁出现水雾 | 说明纸张燃烧有水生成 |
| 再将一个内壁蘸有澄清石灰水的烧杯罩在火焰上方 | 澄清的石灰水变浑浊 | 说明纸张燃烧有二氧化碳生成 |
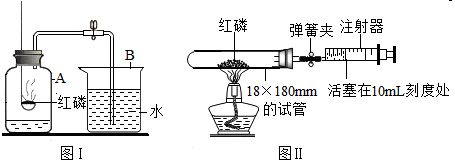 某化学兴趣小组对教材中“测定空气里氧气含量”的实验(见图I)进行了大胆改进,设计图(Ⅱ)(选用容积为45mL的18×180mm的试管作反应容器)实验方案进行,收到了良好的效果.请你对比分析下面图I、图Ⅱ实验,回答下列有关问题:
某化学兴趣小组对教材中“测定空气里氧气含量”的实验(见图I)进行了大胆改进,设计图(Ⅱ)(选用容积为45mL的18×180mm的试管作反应容器)实验方案进行,收到了良好的效果.请你对比分析下面图I、图Ⅱ实验,回答下列有关问题: