题目内容
14.化学与生活、生产、科技紧密相关:(一)化学与生活
(1)人体含量最高的元素是O(填元素符号),加碘食盐中的碘是指元素(填“单质”或“元素”),
构成氯化钠的阳离子是Na+,食用加碘食盐可预防B(填“A”或“B”) A.侏儒症 B.甲状腺疾病;
(2)铝的金属活动性比铁的强(填“强”或“弱”),空气中,铝比铁具有更好的抗腐蚀性,原因是
4Al+3O2═2Al2O3(用化学方程式解释);
(3)小强妈为小强中考预拟得的食谱:主食:馒头;副食:红烧排骨、清蒸鱼;饮料:牛奶,从营养学角度考虑,你建议食谱中增加:D(填序号)
A.油饼 B.红烧豆腐 C.炒鸡蛋 D.凉拌黄瓜
(二)化学与科技
(1)2017年5月18号,我国成功在南海完成可燃冰的试采工作,可燃冰的主要成分是甲烷,
甲烷燃烧的化学方程式是CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(2)“正渗透法”是航天飞机上利用特质半透膜进行污水处理的新方法.这种半透膜允许水分子通过,同时阻止蛋白质、糖等分子通过,该原理与下列常用净水方法在原理上最接近的是C(填序号) A.吸附 B.沉降 C.过滤 D.蒸馏.
分析 (一)(1)根据人体内元素的含量排序分析回答;加碘食盐的“碘”不能以单质、分子、原子形式存在,一般以无机盐类物质存在,指的是元素;根据常见化学用语(分子符号、离子符号等)的书写方法分析回答;根据碘的生理功能、缺乏症等进行分析解答;
(2)根据金属的活动性以及化学方程式的写法来分析解答;
(3)根据人体所需六大营养素的种类、食物来源和合理膳食的原则进行分析;
(二)(1)根据甲烷燃烧生成二氧化碳和水,写出反应的化学方程式即可;
(2)“正渗透法”中的半透膜是允许小分子通过,阻止大分子物质通过的.
解答 解:(一)(1)人体内含量较多的元素有11种,排序为:氧、碳、氢、氮、钙、碗、钾、硫、钠、氯、镁由此可知,人体中含量最高的元素是氧元素;食品、药品、营养品、矿泉水等物质中的“碘、氟、钙、铁、锌”等不能以单质、分子、原子形式存在,而是指元素.故加碘食盐中的“碘”是指元素;构成氯化钠的阳离子是钠离子,其离子符号为:Na+;碘是合成甲状腺激素的主要元素,缺乏会患甲状腺肿大,食用加碘食盐可预防甲状腺疾病.
故答案为:O;元素;Na+;B;
(2)在金属活动性顺序中,铝排在铁的前面,所以铝比铁活泼;铝的活动性比铁强,铝易被氧化生成致密的氧化铝保护膜,起到保护作用,其反应的化学方程式为:4Al+3O2═2 Al2O3;
故答案为:强;4Al+3O2═2 Al2O3;
(3)从提供的食谱可以看出该食谱中含有的营养成分主要是糖类、蛋白质、脂肪及水分与无机盐,缺少维生素,所以应该增加富含维生素的蔬菜类食品凉拌黄瓜.
故答案为:D;
(二) (1)甲烷燃烧生成二氧化碳和水,反应的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
故答案为:CH4+2 O2$\frac{\underline{\;点燃\;}}{\;}$2H2O+CO2;
(2)过滤是它根据滤纸能够透过液体和溶于液体的物质的特殊功能,将混合物分离开来的.滤纸的功能相当于“正渗透法”中的半透膜的功能;
故答案为:C.
点评 本题通考查了一些化学知识,体现了化学就在我们身边,生活中处处有化学,由于于促进化学的学习.

 阅读快车系列答案
阅读快车系列答案| A. | KNO3 | B. | CO(NH2)2 | C. | K2CO3 | D. | Ca3(PO4)2 |
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 |
| 溶解度/g | 7 | 12.5 | 21.5 | 40 | 49 | 46 | 43.6 |
(2)40℃时100g 水中溶有 48g 碳酸钠,欲将其变为饱和溶液,可采用的方法有ABC.
A.加入少量碳酸钠至有固体剩余 B.恒温蒸发少量水分至有少量固体产生
C.降温至有少量碳酸钠结晶 D.升温至有少量碳酸钠结晶.
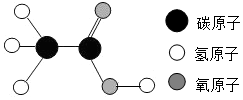
| A. | 乙酸是一种有机化合物 | B. | 乙酸的相对分子质量为60 | ||
| C. | 乙酸中碳的质量分数最大 | D. | 1个乙酸分子中有8个原子 |
| A. | 用白磷和红磷探究可燃物燃烧的条件 | |
| B. | 用紫色石蕊溶液鉴别稀硫酸和氢氧化钠溶液 | |
| C. | 用Mg、Zn和稀盐酸比较Mg、Zn的金属活动性强弱 | |
| D. | 用MnO2、CuO和过氧化氢溶液,比较MnO2、CuO的催化效果 |