题目内容
17.回答下列问题:(1)钠在氯气中燃烧的化学方程式为2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl,反应中钠元素的化合价由0价变为+1价.
(2)上述反应说明燃烧不一定(填“一定”或“不一定”)需要氧气;少量金属钠着火,可以用沙子盖灭,其主要原理是隔绝氧气.
(3)金属钠能与水反应生成氢氧化钠和氢气.请写出该反应的化学方程式2Na+2H2O=2NaOH+H2↑.
分析 (1)钠在氯气中燃烧生成氯化钠,结合单质中元素的化合价为0、在化合物中正负化合价代数和为零,进行分析解答.
(2)根据钠在氯气中燃烧生成氯化钠,结合灭火的原理进行分析解答.
(3)金属钠能与水反应生成氢氧化钠和氢气,写出反应的化学方程式即可.
解答 解:(1)钠在氯气中燃烧生成氯化钠,燃烧的化学方程式为2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl;单质中元素的化合价为0,Na属于单质,故钠元素的化合价为0;氯化钠中氯元素显-1价,钠元素显+1价;反应中钠元素的化合价由0价变为+1价.
(2)钠在氯气中燃烧生成氯化钠,说明燃烧不一定需要氧气;少量金属钠着火,可以用沙子盖灭,利用的是隔绝氧气的灭火原理.
(3)金属钠能与水反应生成氢氧化钠和氢气,反应的化学方程式为:2Na+2H2O=2NaOH+H2↑.
故答案为:(1)2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl;0;+1;(2)不一定; 隔绝氧气;(3)2Na+2H2O=2NaOH+H2↑
点评 本题难度不大,掌握燃烧的条件、灭火的原理、化学方程式的书写方法、化合价的原则是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.根 据 氯 元 素 化 合 价 不 同,有 关 物 质 按 照 一 定 的 规 律 可 排 列 为:①NaCl ②Cl2 ③HClO
④R⑤Cl2O7,则 R 可以是下列物质中的( )
④R⑤Cl2O7,则 R 可以是下列物质中的( )
| A. | KClO3 | B. | HClO2 | C. | Ca(ClO)2 | D. | HClO4 |
1.下列说法正确的是( )
| A. | 金秋十月,丹桂飘香,是因为分子间存在着间隔 | |
| B. | 在化学变化中,分子可以分成原子,原子又可以结合成新的分子 | |
| C. | 水受热变成水蒸气的过程中体积变大,是因为水分子体积变大 | |
| D. | 不同元素的原子的区别是原子的最外层电子数不同 |
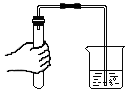 检查装置气密性温度升高,分子间间隔变大.
检查装置气密性温度升高,分子间间隔变大.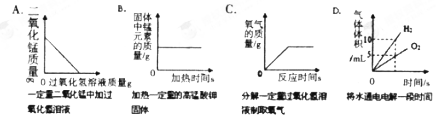
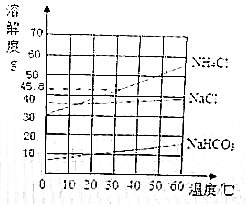 如图是氯化钠、氯化铵和碳酸氢钠三种物质的溶解度曲线,分析曲线回答问题:
如图是氯化钠、氯化铵和碳酸氢钠三种物质的溶解度曲线,分析曲线回答问题: