题目内容
19.不纯的镁12克与足量稀硫酸反应,产生1.2克氢气,则镁中可能含有的一种金属杂质是铝.分析 镁和稀硫酸反应生成硫酸镁和氢气,铝和稀硫酸反应生成硫酸铝和氢气,根据反应的化学方程式及其质量关系可以判断相关方面的问题.
解答 解:镁、铝和稀硫酸反应的化学方程式及其质量关系为:
Mg+H2SO4═MgSO4+H2↑,2Al+3H2SO4═Al2(SO4)3+3H2↑,
24 2 54 6
由以上质量关系可知,12g镁完全和稀硫酸反应生成氢气的质量为:(12g×2)÷24=1g,12g铝完全和稀硫酸反应生成氢气的质量为:
(12g×6)÷54=1.3g,当12g镁和铝的混合物按一定比例混合时,与足量稀硫酸反应生成的氢气质量可能是1.2g,则镁中可能含有的一种金属杂质是铝.
故填:铝.
点评 本题主要考查根据金属混合物与酸反应产生氢气的质量偏大金属的可能组成问题,比较复杂,只要找出一种可能即可,不要求全部罗列.

练习册系列答案
相关题目
3.对于化学式“H2O”的各种表述错误的是( )
| A. | 表示水这种物质 | |
| B. | 表示水分子由氢元素和氧元素组成 | |
| C. | 表示1个水分子 | |
| D. | 表示1个水分子由2个氢原子和1个氧原子构成 |
7.某学生用托盘天平称量食盐,误把食盐放在右盘,而把砝码放在左盘,称得食盐为10.5克(1克以下用游码).若按正确的称量,该学生所称食盐的质量为( )
| A. | 10.5克 | B. | 9.5克 | C. | 10克 | D. | 11.5克 |
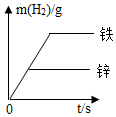
4.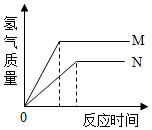 等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如右图所示,下列叙述正确的是( )
等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如右图所示,下列叙述正确的是( )
 等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如右图所示,下列叙述正确的是( )
等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如右图所示,下列叙述正确的是( )| A. | M、N两种金属中较活泼的是N | B. | 生成H2的速率N>M | ||
| C. | 相对原子质量较大的是N | D. | 生成H2的质量M<N |
9.推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | CO2和SO2都能和NaOH溶液反应,CO也能和NaOH溶液反应 | |
| B. | CO和C都能和CuO反应生成Cu,有还原性,H2也能相CuO反应生成Cu,也有还原性 | |
| C. | 活泼金属和盐酸反应生成气体,和盐酸反应生成气体的物质不一定是活发金属 | |
| D. | 氢氧化钙和氢氧化钠都属于碱,都含有金属元素,所以碱都含有金属元素 |
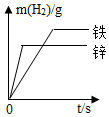
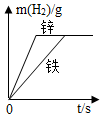
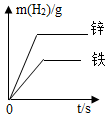
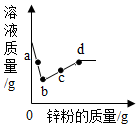 向一定量的硝酸银和硝酸铜的混合溶液中加入锌粉,所得溶液的质量与加入锌粉质量关系如图,请分析a点时溶液中有哪些溶质?c点时过滤能得到哪些固体?b~d段溶液质量增加的原因是什么?
向一定量的硝酸银和硝酸铜的混合溶液中加入锌粉,所得溶液的质量与加入锌粉质量关系如图,请分析a点时溶液中有哪些溶质?c点时过滤能得到哪些固体?b~d段溶液质量增加的原因是什么?