题目内容
5.铜火锅是深受人们喜爱的传统产品,但铜制品放置较长时间表面会形成一种绿色有毒的物质.某化学兴趣小组的同学为探究其成分,从一个久置的废弃铜火锅上取下一些绿色固体进行实验.【提出问题】绿色固体是什么?
【查阅资料】碱式碳酸铜[Cu2(OH)2CO3]是绿色固体,受热分解生成三种物质.
【进行实验】
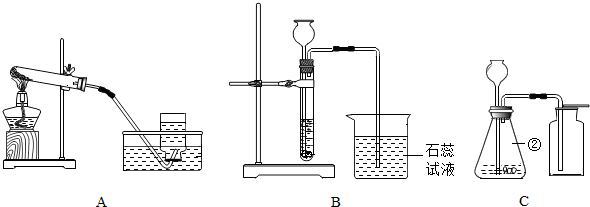
(1)取少量绿色固体于一支洁净的试管中,加热后,观察到试管口有小液滴出现,说明反应后有水生成;澄清石灰水变浑浊,说明反应后生成二氧化碳;同时观察到试管中绿色固体变为黑色.
(2)为了探究黑色固体的成分,同学们进行了实验,操作是取适量固体粉末于试管中,然后加入适量稀盐酸,现象是黑色固体溶解,溶液变蓝,化学方程式为CuO+2HCl═CuCl2+H2O.
【得出结论】通过实验结合资料分析可知绿色固体是碱式碳酸铜.
【表达交流】结合铁生锈的条件,经过讨论,同学们认为铜制品锈蚀的原因可能是铜与空气中的氧气以及水蒸气、二氧化碳接触反应的结果.大家认为防止金属锈蚀可采取的措施有在金属表面涂一层油漆(写出一条即可).
分析 【进行实验】
二氧化碳能使澄清石灰水变浑浊;
氧化铜能和稀盐酸反应生成氯化铜和水,氯化铜溶液是蓝色的;
【表达交流】
铜和空气的二氧化碳、水蒸气和氧气同时接触时容易生锈.
解答 解:【进行实验】
(1)取少量绿色固体于一支洁净的试管中,如图.加热后,澄清石灰水变浑浊,说明反应后生成二氧化碳.
故填:二氧化碳.
(2)为了探究黑色固体的成分,同学们进行了实验,操作是取适量固体粉末于试管中,然后加入适量稀盐酸,现象是黑色固体溶解,溶液变蓝,说明黑色粉末是氧化铜,氧化铜和稀盐酸反应生成氯化铜和水,反应的化学方程式为:CuO+2HCl═CuCl2+H2O.
故填:取适量固体粉末于试管中,然后加入适量稀盐酸;黑色固体溶解,溶液变蓝;CuO+2HCl═CuCl2+H2O.
【表达交流】
结合铁生锈的条件,经过讨论,同学们认为铜制品锈蚀的原因可能是铜与空气中的氧气以及水蒸气、二氧化碳接触反应的结果;
大家认为防止金属锈蚀可采取的措施有:保持金属表面干燥,在金属表面镀一层金属,在金属表面涂一层油漆等,都可以防止金属生锈.
故填:水蒸气、二氧化碳;在金属表面涂一层油漆.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
4.归纳推理是学习化学的重要方法之一.下列有关实验事实和实验结论正确的是( )
| 选项 | 实验事实 | 实验结论 |
| A | 某气体能使燃着的木条熄灭 | 该气体一定是二氧化碳 |
| B | 常温下,测得某溶液的pH=10 | 该溶液一定呈碱性 |
| C | 溶液具有均一、稳定的特征 | 均一、稳定的液体一定是溶液 |
| D | 某物质可以导电 | 该物质一定是石墨 |
| A. | A | B. | B | C. | C | D. | D |
16.单质碘呈紫黑色晶体,易升华,有毒性和腐蚀性,碘单质遇淀粉水溶液会变蓝色,主要用于制药物、染料、碘酒、试纸和碘化合物等,碘是人体的必需微量元素之一.上述对碘的描述中,没有涉及到的是( )
| A. | 物理性质 | B. | 制法 | C. | 用途 | D. | 化学性质 |
10. 钾是人体生命和植物生长所必須的元素,如图是从元家周期表中得出的部分信息.下列关于钾元素的有关叙述错误的是( )
钾是人体生命和植物生长所必須的元素,如图是从元家周期表中得出的部分信息.下列关于钾元素的有关叙述错误的是( )
 钾是人体生命和植物生长所必須的元素,如图是从元家周期表中得出的部分信息.下列关于钾元素的有关叙述错误的是( )
钾是人体生命和植物生长所必須的元素,如图是从元家周期表中得出的部分信息.下列关于钾元素的有关叙述错误的是( )| A. | 钾元素属于金属元素 | B. | 钾元素的原子序数为19 | ||
| C. | 钾元素的相对原子质量为39.10 | D. | 钾原子核内中子数为19 |
17.下列说法正确的是( )
| A. | 棉、羊毛,塑料等都属于天然有机高分子材料 | |
| B. | 食用加碘食盐和强化铁酱油可补充某些人体必需微量元素 | |
| C. | 用甲醛水溶液浸泡水产品以防止腐烂 | |
| D. | 铁制品表面涂“银粉(铝粉)”防生绣,是由于铝的化学性质比铁稳定 |
15.下列物质分类合理的是( )
| A. | 合 金------不锈钢、锌 | B. | 碳单质-----金刚石、石墨、C60 | ||
| C. | 化石燃料-----煤、氢气、天然气 | D. | 天然材料-----涤纶、棉花 |