题目内容
 某校化学小组同学从家中带来淀粉、食盐、纯碱、泡打粉、去污粉和部分变质的熟石灰6种固体物质.老师从中取出任意3种并编号,让小组同学通过实验确认分别为哪种固体.
某校化学小组同学从家中带来淀粉、食盐、纯碱、泡打粉、去污粉和部分变质的熟石灰6种固体物质.老师从中取出任意3种并编号,让小组同学通过实验确认分别为哪种固体.【查阅资料】
①该去污粉主要成分为碳酸钠和碳酸钙
②该泡打粉的主要成分是碳酸氢钠和有机酸
③熟石灰变质的原因是因为其吸收了空气中的二氧化碳.
【实验准备】
为顺利完成任务,小组同学在老师指导下进行了如下预备实验.部分现象记录如下:
| 实验1 取样,加足量水充分溶解 | 实验2 取样,加入适量稀盐酸 | |
| 淀粉 | 白色浑浊,试管底部有不溶物 | 无明显现象 |
| 泡打粉 | 有气体产生,试管底部有白色不溶物 | 有气体产生 |
小组同学对老师提供的三种固体进行实验探究.部分现象记录如下:
| 实验1 取样,加足量水充分溶解 | 实验2 取样,加入适量稀盐酸 | 实验3 取实验1上层清液,加入3滴酚酞溶液 | |
| 固体Ⅰ | 有气体产生,试管底部有白色不溶物 | 有气体产生 | |
| 固体Ⅱ | 固体溶解,形成无色溶液 | 有气体产生 | 溶液变红 |
| 固体Ⅲ | 有白色浑浊,试管底部有白色不溶物 | 有气体产生 | 溶液变红 |
(1)固体Ⅱ、Ⅲ加水形成的溶液pH
(2)分析以上实验现象得知,固体Ⅰ是
(3)小组同学通过讨论认为固体Ⅲ不能确定.请你设计确认该固体的实验方案
考点:物质的鉴别、推断,碱的化学性质,溶液的酸碱性与pH值的关系,盐的化学性质
专题:物质的鉴别题
分析:【得出结论】
(1)有表中信息可知固体Ⅱ、Ⅲ加水形成的溶液pH;
(2)根据表中的实验信息可解答;
(3)根据去污粉和部分变质的熟石灰的性质解答.
(1)有表中信息可知固体Ⅱ、Ⅲ加水形成的溶液pH;
(2)根据表中的实验信息可解答;
(3)根据去污粉和部分变质的熟石灰的性质解答.
解答:解:【得出结论】(1)固体Ⅱ、Ⅲ加水形成的溶液都能使酚酞变红色,说明水溶液显碱性,故溶液pH>7;
(2)分析以上实验现象得知,取样,加足量水充分溶解,有气体产生,试管底部有白色不溶物,取样,加入适量稀盐酸,有气体产生;这些与实验准备中泡打粉性质一样,所以固体Ⅰ是泡打粉;固体Ⅱ的性质是纯碱的性质,故固体Ⅱ是纯碱;
(3)小组同学通过讨论认为固体Ⅲ不能确定,设计确认该固体的实验方案:取少量固体Ⅲ于烧杯中,加入足量的水溶解,过滤,向滤液中加入足量稀盐酸,若有气体逸出,则固体Ⅲ为去污粉;若无气体逸出,则为部分变质的熟石灰.
故答案为:(1)>;
( 2)泡打粉;纯碱(或Na2CO3);
(3)取少量固体Ⅲ于烧杯中,加入足量的水溶解,过滤,向滤液中加入足量稀盐酸,若有气体逸出,则固体Ⅲ为去污粉;若无气体逸出,则为部分变质的熟石灰.
(2)分析以上实验现象得知,取样,加足量水充分溶解,有气体产生,试管底部有白色不溶物,取样,加入适量稀盐酸,有气体产生;这些与实验准备中泡打粉性质一样,所以固体Ⅰ是泡打粉;固体Ⅱ的性质是纯碱的性质,故固体Ⅱ是纯碱;
(3)小组同学通过讨论认为固体Ⅲ不能确定,设计确认该固体的实验方案:取少量固体Ⅲ于烧杯中,加入足量的水溶解,过滤,向滤液中加入足量稀盐酸,若有气体逸出,则固体Ⅲ为去污粉;若无气体逸出,则为部分变质的熟石灰.
故答案为:(1)>;
( 2)泡打粉;纯碱(或Na2CO3);
(3)取少量固体Ⅲ于烧杯中,加入足量的水溶解,过滤,向滤液中加入足量稀盐酸,若有气体逸出,则固体Ⅲ为去污粉;若无气体逸出,则为部分变质的熟石灰.
点评:利用实验鉴别物质是一类难度较大的化学题目.解答该类题目时,要弄清涉及的各种物质的性质,然后根据实验步骤逐步确定物质.
注意题目中的要求,弄清是要填物质名称还是化学式,或者是序号.这也是一个易错点.
注意题目中的要求,弄清是要填物质名称还是化学式,或者是序号.这也是一个易错点.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
某金属加工厂生产过程中的废液含有少量的硝酸银和硝酸铜,为回收利用资源和防止污染,该厂向废液中加入一定量的铁粉,反应停止后过滤,向滤渣中加入少量的稀盐酸,无气泡产生,则下列有关说法正确的是( )
| A、滤出的固体中一定只含银 |
| B、滤出的固体中一定含有银和铜,一定不含铁 |
| C、滤液中一定含有硝酸亚铁,可能含有硝酸银和硝酸铜 |
| D、滤液中一定含有硝酸亚铁,一定没有硝酸银 |
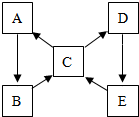 已知A、B、C、D、E是初中化学中常见的五种物质,且都含有同一种金属元素,化合物中金属元素的化合价均为+2.其中A是紫红色金属,在空气中加热后生成黑色物质B;C溶液与一种金属反应可得到A,与氯化钡溶液反应可得到D,同时有白色沉淀生成;D溶液中加入少量的氢氧化钠溶液得到E.它们在一定条件下的转化关系如图所示(→表示转化,部分反应物、生成物及反应条件略去).请回答下列问题:
已知A、B、C、D、E是初中化学中常见的五种物质,且都含有同一种金属元素,化合物中金属元素的化合价均为+2.其中A是紫红色金属,在空气中加热后生成黑色物质B;C溶液与一种金属反应可得到A,与氯化钡溶液反应可得到D,同时有白色沉淀生成;D溶液中加入少量的氢氧化钠溶液得到E.它们在一定条件下的转化关系如图所示(→表示转化,部分反应物、生成物及反应条件略去).请回答下列问题:


