题目内容
现有一包固体粉末,可能是碳酸钠、硫酸钠、硫酸铜、氯化钠中的一种或几种,为了测定其组成,取适量样品进行下列实验,请根据实验现象判断:
(1)取样品溶于水,得到无色澄清溶液,则此固体粉末中一定没有 _________ .
(2)取上述溶液适量,滴加过量的氯化钡溶液,出现白色沉淀.过滤,向沉淀中加入过量的稀硝酸,沉淀部分消失并产生气泡,则此固体粉末中一 定含有 _________ .
定含有 _________ .
(3)取步骤哦(2)试验后的滤液,加入稀硝酸化后,再加入硝酸银溶液,出现白色沉淀.由此某同学得出此固体粉末中一定含有氯化钠.你认为此结论是否正确? _________ (填“是”或“否”).请说明理由 _________ .
解析:题中所给的 各种物质都溶于水,硫酸铜在溶液中显蓝色,碳酸根离子和钡离子会生成碳酸钡沉淀,碳酸钡沉淀会溶于酸生成二氧化碳气体,硫酸根离子和钡离子会生成硫酸钡沉淀,硫酸钡沉淀不溶于酸,氯离子和银离子会生成不溶于酸的氯化银沉淀.
各种物质都溶于水,硫酸铜在溶液中显蓝色,碳酸根离子和钡离子会生成碳酸钡沉淀,碳酸钡沉淀会溶于酸生成二氧化碳气体,硫酸根离子和钡离子会生成硫酸钡沉淀,硫酸钡沉淀不溶于酸,氯离子和银离子会生成不溶于酸的氯化银沉淀.
(1)取样品溶于水,得到无色澄清溶液,则此固体粉末中一定没有:硫酸铜;
(2)取上述溶液适量,滴加过量的氯化钡溶液,出现白色沉淀,过滤,向沉淀中加入过量的稀硝酸,沉淀部分消失并产生气泡,所以此固体粉末中一定含有:硫酸钠、碳酸钠;
(3)取步骤(2)试验后的滤液,加入稀硝酸化后,再加入硝酸银溶液,出现白色沉淀,只能判断是氯离子和银离子生成的氯化银沉淀,但是氯化钡也会提供氯离子,氯化钠也会提供氯离子,所以不能判断固体粉末中一定含有氯化钠,理由是:在步骤(2)中加入的氯化钡,也会引入氯离子,不能氯离子时氯化钠提供的,还是氯化钡提供的.
故答案为:(1)硫酸铜;
(2)硫酸钠、碳酸钠;
(3 )否,在步骤(2)中加入的氯化钡,也会引入氯离子,不能确定氯离子是氯化钠提供的,还是氯化钡提供的.
)否,在步骤(2)中加入的氯化钡,也会引入氯离子,不能确定氯离子是氯化钠提供的,还是氯化钡提供的.

 53随堂测系列答案
53随堂测系列答案下列有关溶液的说法中正确的是( )
|
| A | 常温下将100mL饱和Ca(OH)2溶液加热到50℃,会使溶液由饱和溶液变为不饱和溶液 |
|
| B | 从浓度为25%的H2SO4溶液中取出10mL,则取出的10mL H2SO4溶液浓度仍为25% |
|
| C | 20℃时,50克水中溶解了18克NaCl,则20℃时NaCl的溶解度为36克 |
|
| D | 将95克KCl溶液蒸干得到5克固体,则原溶液中KCl的浓度为5% |
下列实验过程与图象描述不相符合的选项是( )
|
| A. |
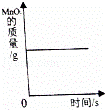
一定温度下,向饱和氢氧化钙溶液中加入氧化钙 |
|
| B. |
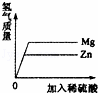
向等质量的镁、锌中同时加入 |
|
| C. |
加热一定量的氯酸钾和二氧化锰混合物制氧气 |
|
| D. |
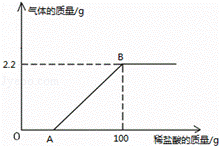
一定量的石灰石加入到足量的稀盐酸中(不考虑水的蒸发、氯化氢的挥发) |
下列说法中,错误的是( )
|
| A. | 二氧化碳可用于灭火 |
|
| B. | 可用pH试纸测定溶液酸碱度 |
|
| C. | 可用灼烧的方法鉴定羊毛、合成纤维 |
|
| D. | 稀释浓硫酸时可将水倒入盛有浓硫酸的烧杯中 |
下列变化属于化学变化的是
| A.酒精燃烧 | B.汽油挥发 | C.风力发电 | D.海水晒盐 |
|
 (1)从微观角度看物质的变化是化学的思维方式之一。下面两幅示意图分别表示生成氯化钠的不同化学反应。请根据图示回答相关问题:
(1)从微观角度看物质的变化是化学的思维方式之一。下面两幅示意图分别表示生成氯化钠的不同化学反应。请根据图示回答相关问题:
|

|
|
|
| ||||||||||
| |||||||||||
| |||||||||||
 | |||||||||||
| |||||||||||
①图1是金属钠与氯气反应生成氯化钠的微观示意图。由图1可知,元素的化学性质与
其微粒的 (填字母序号)有密切关系。
A.最外层电子数 B.内层电子数 C.电子层数 D.核电荷数
②图2描述了NaOH溶液与盐酸反应的微观实质是 。
(2)用质量分数为6%的氯化钠溶液(密度为1.04g/cm3),配制100g质量分数为3%的
氯化钠溶液。配制过程为:
①计算(计算结果保留一位小数) :需6%的氯化钠溶液 mL(计算的依据
:需6%的氯化钠溶液 mL(计算的依据
是 ),水 g。
②量取;③ ;④装瓶、贴标签。
 请写出该反应的化学方程式: _________ .
请写出该反应的化学方程式: _________ .