题目内容
2.蛋白质是由氨基酸组成的,氨基酸中有一种叫丙氨酸的,其结构式为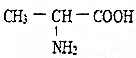 ,它与氢氧化钠反应的化学方程式为:
,它与氢氧化钠反应的化学方程式为: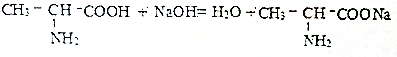
请你计算:
(1)丙氨酸中碳氢两元素的质量比;
(2)丙氨酸中氮元素的质量分数;
(3)17.8g丙氨酸与100g某氢氧化钠溶液正好完全反应,试计算该氢氧化钠溶液溶质的质量分数.
分析 根据物质的化学式来分析,根据丙氨酸的化学式;利用各元素的质量比为各元素相对原子质量和的比即可求得丙氨酸中碳氢质量比;元素的质量分数就是该元素的相对原子质量与原子个数的乘积与相对分子质量的比值;根据反应结合提供的数据解答即可.
解答 解:丙氨酸的化学式为:C3H7O2N,
(1)丙氨酸中碳氢元素间的质量比为=(12×3):(1×7)=36:7,故填:36:7;
(2)丙氨酸中氮元素的质量分数=$\frac{14}{12×3+1×7+16×2+14}×100%$≈15.7%;
(3)丙氨酸与氢氧化钠反应的化学方程式为:C3H7O2N+NaOH=C3H6O2NNa+H2O
设氢氧化钠的质量为x
C3H7O2N+NaOH=C3H6O2NNa+H2O
89 40
17.8g x
$\frac{89}{40}=\frac{17.8g}{x}$ x=8g
氢氧化钠溶液的质量分数为:$\frac{8g}{100g}×100%$=8%
答:(1)丙氨酸中碳氢两元素的质量比为36:7;
(2)丙氨酸中氮元素的质量分数为15.7%;
(3)该氢氧化钠溶液溶质的质量分数为8%.
点评 本题考查的是根据化学式的计算以及根据化学方程式的计算,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
17.在一密闭容器里放入四种物质,使其在一定条件下充分反应,测得数据如下:
则下列表述正确的是( )
| 四种物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 25 | 15 | 1 | 5 |
| 反应后质量(g ) | 11 | 未测 | 1 | 22 |
| A. | 未测值为2 | B. | 甲和乙反应的质量比为25:15 | ||
| C. | 乙全部发生了反应 | D. | 丙可能是催化剂 |
14.为了除去物质内的杂质,需选用适当的除杂方法,其中不正确的是( )
| 选项 | 物质 | 所含杂质 | 除杂方法 |
| A | H2 | HCl | 先通过NaOH溶液,再通过浓硫酸 |
| B | CO | CO2 | 通过碱石灰(CaO和NaOH固体) |
| C | C | Fe | 加入过量的稀盐酸,过滤,洗涤,干燥 |
| D | NaOH溶液 | Na2CO3 | 加入稀盐酸至不再产生气泡 |
| A. | A | B. | B | C. | C | D. | D |
12.下列类推正确的是( )
| A. | 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐 | |
| B. | 置换反应一定有单质生成,所以有单质生成的反应一定是置换反应 | |
| C. | 燃烧一般都伴随发光、放热现象,所以有发光、放热的现象就是燃烧 | |
| D. | 根据溶解度曲线图,判断从溶液中获得晶体的方法 |