题目内容
6.探究氯酸钾和二氧化锰制氧气实验中反应物与催化剂的最佳质量比.实验中采用如图实验装置,取20g氯酸钾,分成10等份,每份2g,分别装入10支试管中.在10支试管中分别加入不同质量的二氧化锰,分别测量二氧化锰与氯酸钾在不同质量比时,生成200mL氧气所用的时间.实验记录的数据如表所示:
| 实验编号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 二氧化锰的质量/g | 0.1 | 0.2 | 0.33 | 0.4 | 0.5 | 0.66 | 1 | 1.3 | 2 | 3 |
| 二氧化锰与氯酸钾的质量比 | 1:20 | 1:10 | 1:6 | 1:5 | 1:4 | 1:3 | 1:2 | 2:3 | 1:1 | 3:2 |
| 生成200mL氧气时间/秒 | 235 | 186 | 162 | 147 | 133 | 117 | 143 | 160 | 211 | 244 |
(1)实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出反应的文字表达式:氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气.
(2)此实验中收集一定体积的氧气宜采取的收集方法是排水法.原因是不易溶于水,收集气体前集气瓶内未装满水,对实验结果没有 (填“有”或“没有”)影响.
(3)分析上述数据,你认为利用此法制氧气,二氧化锰与氯酸钾的最佳质量比为1:3.
(4)利用双氧水和二氧化锰的混合物制氧气比加热氯酸钾和二氧化锰混合物制氧气更好.请写出前者的两个优点操作简便、节能.
(5)催化剂能影响化学反应速率,温度、反应物的浓度、接触面积等也会对化学反应速率带来影响.分析上表数据,结合影响化学反应速率的因素分析:
①当二氧化锰与氯酸钾的质量比高于最佳质量比时,反应速度变低的原因是:二氧化锰用量多,导致反应物氯酸钾的质量分数变小.
②当二氧化锰与氯酸钾的质量比低于最佳质量比时,反应速度变低的原因是:二氧化锰用量少,导致氯酸钾与二氧化锰的接触面积变小.
分析 (1)根据加热氯酸钾与二氧化锰生成氯化钾和氧气进行解答;
(2)根据氧气的溶解性和排出水的体积即为气体体积来分析;
(3)根据图表中的数据分析,所用时间少的就是反应速率快的;
(4)双氧水和二氧化锰混合制氧气不需加热,可以节能等分析;
(5)根据反应速度的影响因素主要是反应物的接触面积;混合物的混合情况考虑,催化剂多了相对来说反应物就少了,反应速度就收到了影响
解答 解:(1)加热氯酸钾与二氧化锰生成氯化钾和氧气,反应的文字表达式:氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气;故填:氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气;
(2)利用排水装置收集的气体应具备的性质是难溶于水;空气不易溶于水,那么排出水的气体即为所收集的气体体积,.
故答案为:不易溶于水;没有;
(3)通过观察图表中的数据可知,二氧化锰与氯酸钾的质量比是 1:3时,所用的时间最少,反应速率最快.
故答案为:1:3;
(4)双氧水和二氧化锰混合制氧气不需加热,可以节能,同时更安全;副产物是水无污染,更环保;价格低廉,操作简便等;
故答案为:操作简便;节能;
(5)①二氧化锰用量过多氯酸钾的质量分数就降低了,反应物的接触面积就少了,就影响了反应速度;
②反应速度的影响因素主要是反应物的接触面积,接触面积越大反应速度就越快,二氧化锰的用量过少与氯酸钾的接触面积就越小,所以反应速度慢;
故答案为:①二氧化锰用量多,导致反应物氯酸钾的质量分数变小;
②二氧化锰用量少,导致氯酸钾与二氧化锰的接触面积变小.
点评 此题探究实验室用二氧化锰与氯酸钾制取氧气时,二氧化锰作催化剂的量要适中,过多或过少反应速率都或受到影响.希望同学们作此试验时注意二氧化锰的用量,节约药品.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.在氧气中燃烧产生“火星四射”现象的物质是( )
| A. | 铁丝 | B. | 镁带 | C. | 红磷 | D. | 木炭 |
11.化学教材“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣.
【提出问题】氧化铁、氧化铜能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
验探究1】
(1)A中产生的气体是氧气
(2)在第③步中,要使剩余物分离必须进行的操作是过滤,必须用到的仪器有铁架台、玻璃棒、烧杯和漏斗,玻璃棒的作用是引流
【实验结论】
(3)实验②、③证明:氧化铁的质量和化学性质在反应前后均没有发生变化,可以作过氧化氢分解的催化剂;
(4)写出氧化铁催化过氧化氢分解的文字表达式过氧化氢$\stackrel{氧化铁}{→}$水+氧气.
【实验评论】
(5)实验设计④的目的是证明氧化铁与二氧化锰哪一个更适合做过氧化氢分解生成氧气的催化剂,若实验④观察到D试管中产生气泡的速率更快,由此你可以得到的结论是二氧化锰更适合做过氧化氢分解生成氧气的催化剂
【知识拓展】
(6)查阅资料得知,CuO、CuSO4、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂,下列有关催化剂的说法中正确的是B
A.催化剂只加快反应速率
B.同一个化学反应可以有多种催化剂
C.MnO2只能作为氧化氢溶液分解的催化剂
D.用作催化剂的物质不可能是其他反应的反应物或生成物.
【提出问题】氧化铁、氧化铜能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
验探究1】
| 实验步骤 | 实验现象 |
| ①分别量取5mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入a g氧化铁粉末,并分别在A、B两支试管中插入带火星的木条,观察现象. | A试管中产生大量气泡,带火星木条复燃,B试管中无明显现象 |
| ②待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管内,如此反复多次实验,观察现象. | 试管中均产生大量气泡,带火星木条均复燃 |
| ③将实验②中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为a g. | / |
| ④分别量取5mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入a g氧化铁粉末,向D试管中加入a g二氧化锰粉末,观察现象. | / |
(2)在第③步中,要使剩余物分离必须进行的操作是过滤,必须用到的仪器有铁架台、玻璃棒、烧杯和漏斗,玻璃棒的作用是引流
【实验结论】
(3)实验②、③证明:氧化铁的质量和化学性质在反应前后均没有发生变化,可以作过氧化氢分解的催化剂;
(4)写出氧化铁催化过氧化氢分解的文字表达式过氧化氢$\stackrel{氧化铁}{→}$水+氧气.
【实验评论】
(5)实验设计④的目的是证明氧化铁与二氧化锰哪一个更适合做过氧化氢分解生成氧气的催化剂,若实验④观察到D试管中产生气泡的速率更快,由此你可以得到的结论是二氧化锰更适合做过氧化氢分解生成氧气的催化剂
【知识拓展】
(6)查阅资料得知,CuO、CuSO4、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂,下列有关催化剂的说法中正确的是B
A.催化剂只加快反应速率
B.同一个化学反应可以有多种催化剂
C.MnO2只能作为氧化氢溶液分解的催化剂
D.用作催化剂的物质不可能是其他反应的反应物或生成物.
15. 右图是M、N两种固体物质的溶解度曲线,下列说法错误的是( )
右图是M、N两种固体物质的溶解度曲线,下列说法错误的是( )
 右图是M、N两种固体物质的溶解度曲线,下列说法错误的是( )
右图是M、N两种固体物质的溶解度曲线,下列说法错误的是( )| A. | M物质的溶解度受温度影响变化较大 | |
| B. | 40℃时,M、N两种物质的溶解度相等 | |
| C. | 升高温度可将M的饱和溶液变为不饱和溶液 | |
| D. | 60℃时,饱和溶液中溶质的质量分数大小关系为N>M |
16.下列由实验现象得到的结论,正确的是( )
| A. | 向某溶液中加BaCl2溶液,生成白色沉淀,说明该溶液中一定含有SO42- | |
| B. | 向某固体中加入稀盐酸,有气泡产生,说明此固体一定是金属 | |
| C. | CaCO3与BaCl2能够发生复分解反应,是因为能生成沉淀 | |
| D. | 向某溶液中滴加无色酚酞试液,酚酞试液变红,说明该溶液显碱性 |

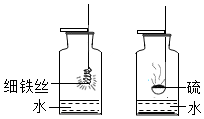 用如图装置做铁丝、硫燃烧的实验.
用如图装置做铁丝、硫燃烧的实验.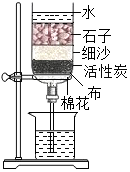 小冬同学制作的简易净水器如图所示:
小冬同学制作的简易净水器如图所示: