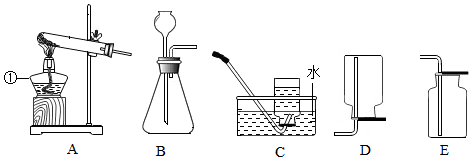
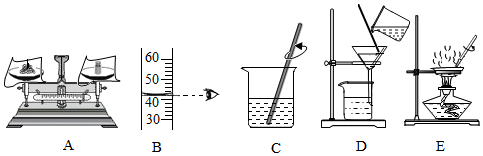
题目内容
11.甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )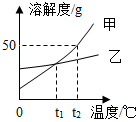
| A. | 甲的溶解度大于乙的溶解度 | |
| B. | t2℃时,甲饱和溶液溶质质量分数为50% | |
| C. | t1℃时,甲、乙两种物质的溶液中,溶质质量分数相等 | |
| D. | 将t2℃时等质量甲、乙的饱和溶液分别降至t1℃,所得溶液中的溶剂质量:甲<乙 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、在一定的温度下比较物质的溶解度,在温度高于t1℃时,甲的溶解度大于乙的溶解度,错误;
B、t2℃时,甲饱和溶液溶质质量分数为$\frac{50g}{100g+50g}×100%≈33.3%≠$50%,错误;
C、t1℃时,甲和乙的溶解度相等,故甲、乙两种物质的饱和溶液中,溶质质量分数相等,错误;
D、t2℃时等质量甲、乙的饱和溶液中,乙的溶剂的质量大于甲,分别降至t1℃,溶剂的质量不变,所得溶液中的溶剂质量:甲<乙,正确;
故选D.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
11.下列有关图标或实验操作正确的是( )
| A. | 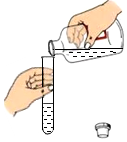 倾倒液体 | B. | 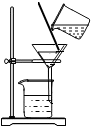 过滤 | C. |  禁止携带火种 | D. | 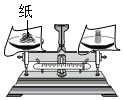 称量NaOH固体 |
8.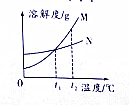 如图是M、N两种固体物质的溶解度曲线.下列说法不正确的是.
如图是M、N两种固体物质的溶解度曲线.下列说法不正确的是.
 如图是M、N两种固体物质的溶解度曲线.下列说法不正确的是.
如图是M、N两种固体物质的溶解度曲线.下列说法不正确的是.| A. | t2℃时,M的溶解度大于N的溶解度 | |
| B. | t1℃时,M和N的饱和溶液中溶质质量分数相等 | |
| C. | M中混有少量的N,可采用降温结晶的方法提纯M | |
| D. | 将t2℃时,等质量的M、N的饱和溶液降温至t1℃,所得溶液中溶质质量大小关系为:M=N |
6.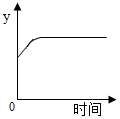 已知:Na2CO3+H2O+CO2═2NaHCO3将二氧化碳气体缓慢通入到一定质量的Na2CO3溶液中,测得变量y随 时间的变化趋势如图所示.变量y可表示的是( )
已知:Na2CO3+H2O+CO2═2NaHCO3将二氧化碳气体缓慢通入到一定质量的Na2CO3溶液中,测得变量y随 时间的变化趋势如图所示.变量y可表示的是( )
 已知:Na2CO3+H2O+CO2═2NaHCO3将二氧化碳气体缓慢通入到一定质量的Na2CO3溶液中,测得变量y随 时间的变化趋势如图所示.变量y可表示的是( )
已知:Na2CO3+H2O+CO2═2NaHCO3将二氧化碳气体缓慢通入到一定质量的Na2CO3溶液中,测得变量y随 时间的变化趋势如图所示.变量y可表示的是( )| A. | 溶剂的质量 | B. | 碳酸钠的质量分数 | ||
| C. | 溶液中碳元素的质量 | D. | 溶液中钠元素的质量 |
16.为了预防H7N9禽流感,养殖户定期会用15%的过氧乙酸溶液对鸡、鸭舍进行消毒.若实验室配制15%的过氧乙酸溶液,下列说法不正确的是( )
| A. | 配制15%的过氧乙酸溶液100克,需要过氧乙酸15克 | |
| B. | 配制时把过氧乙酸倒入量筒中搅拌溶解 | |
| C. | 量筒量取水时,如果视线俯视,则配制溶质的质量分数偏大 | |
| D. | 配制好的溶液装入试剂瓶中,盖好瓶塞并贴上标签 |
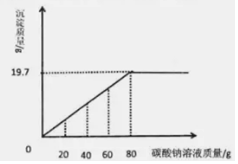 实验室有一包氯化钡和氯化钠的固体混合物32.5g,完全溶于141.2g水中,向其中逐滴加入碳酸钠溶液,反应过程中生成沉淀等质量与所加碳酸钠溶液质量的关系如图所示.
实验室有一包氯化钡和氯化钠的固体混合物32.5g,完全溶于141.2g水中,向其中逐滴加入碳酸钠溶液,反应过程中生成沉淀等质量与所加碳酸钠溶液质量的关系如图所示. 元旦联欢会上,雯雯拿出一幅画(如图所示),表演了一个化学魔术.
元旦联欢会上,雯雯拿出一幅画(如图所示),表演了一个化学魔术.