题目内容
11.将100克质量分数为17.1%的氢氧化钡溶液与100克质量分数为7.3%的盐酸溶液混合后,再加入下列物质:①AgNO3 ②Ba(NO3)2 ③NaOH ④Na2SO4,一定能发生反应的是( )| A. | ①③ | B. | ①④ | C. | ②④ | D. | ③④ |
分析 根据氢氧化钡与稀盐酸反应的化学方程式,判断完全反应后剩余的是哪一种溶液,结合酸或碱的化学性质,进行分析判断.
解答 解:100克质量分数为17.1%的氢氧化钡溶液含有氢氧化钡的质量为100g×17.1%=17.1g;100克质量分数为7.3%的盐酸溶液中含有氯化氢的质量为100g×7.3%=7.3g.
反应中消耗盐酸酸与氢氧化钠的质量比关系如下:
Ba(OH)2+2HCl═BaCl2+2H2O
171 73
可知,171份质量的盐酸与73份质量的氢氧化钠恰好完全反应,则100克质量分数为17.1%的氢氧化钡溶液与100克质量分数为7.3%的盐酸溶液混合后,恰好完全反应,所得溶液是氯化钡溶液.
①氯化钡能与AgNO3反应生成氯化银沉淀和硝酸钡.
②氯化钡不与硝酸钡溶液反应.
③氯化钡不与氢氧化钠溶液反应.
④氯化钡与硫酸钠溶液反应生成硫酸钡沉淀和氯化钠.
故①④一定能发生反应.
故选:B.
点评 本题难度不大,掌握中和反应应用,根据化学方程式的计算判断出反应后剩余的物质是正确解答本题的关键.

练习册系列答案
相关题目
2.提倡“免赠贺卡”,“免用一次性木筷”的出发点是( )
| A. | 减少个人经济开支 | B. | 节约木材、保护森林 | ||
| C. | 减少固体垃圾 | D. | 移风易俗 |
16.“超临界水”因具有许多优良特性而被科学家追捧,它是指当温度和压强达到一定值时,水的液态和气态完全交融在一起的液体.下列有关“超临界水”的说法正确的是( )
| A. | 它是一种混合物 | |
| B. | 它是一种不同于水的新物质 | |
| C. | 它的化学性质与蒸馏水相同 | |
| D. | 它的一个分子由4个氢原子和2个氧原子构成 |
3.把等质量、等质量分数的稀盐酸和氢氧化钠溶液混合反应后,所得溶液中的溶质是( )
| A. | NaCl | B. | NaCl和HCl | C. | NaCl和NaOH | D. | NaCl和NaOH、HCl |
20.生活中处处充满化学.下列各组知识的总结完全正确的一组是( )
| A | ①分子可分,原子不可分 ②原子的质量主要集中在原子核上 | B | ①食用加碘盐可以预防人体贫血 ②蔬菜能为人体提供多种维生素 |
| C | ①洗洁精清除油污利用了乳化作用 ②硝酸铵溶于水使溶液的温度降低 | D | ①木柴架空有利于木柴的完全燃烧 ②用细沙灭火降低了可燃物着火点 |
| A. | A | B. | B | C. | C | D. | D |
1.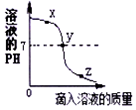 盐酸和滴有酚酞的氢氧化钠溶液发生反应时,溶液pH变化如图所示,有关说法不正确的是( )
盐酸和滴有酚酞的氢氧化钠溶液发生反应时,溶液pH变化如图所示,有关说法不正确的是( )
 盐酸和滴有酚酞的氢氧化钠溶液发生反应时,溶液pH变化如图所示,有关说法不正确的是( )
盐酸和滴有酚酞的氢氧化钠溶液发生反应时,溶液pH变化如图所示,有关说法不正确的是( )| A. | 该实验是向氢氧化钠溶液中滴入盐酸 | |
| B. | x点时,溶液中只含有一种溶质 | |
| C. | y点表示盐酸和氢氧化钠恰好完全反应 | |
| D. | y点和z点时,溶液均呈现无色 |