题目内容
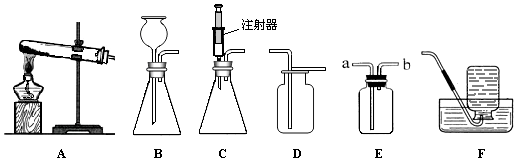
1.现有下列仪器:A、托盘天平 B、量筒 C、酒精灯 D、药匙 E、胶头滴管F、玻璃棒 G、烧杯.欲配置50克18%的食盐水,请根据要求回答:﹙1﹚实验中不需要用到的一种仪器(填序号)C;
﹙2﹚实验步骤可依次概括为计算、称量、溶解等三步;
﹙3﹚需用量筒取水41毫升.
分析 (1)根据配制溶质质量分数一定的溶液的步骤,分析确定需要的仪器.
(2)根据配制溶质质量分数一定的溶液的基本步骤,进行分析解答.
(3)溶质质量=溶液质量×溶质的质量分数,溶剂质量=溶液质量-溶质质量,进行分析解答.
解答 解:(1)配制50克18%的食盐水,首先计算配制溶液所需食盐和水的质量,再称量所需的食盐和量取水,最后进行溶解;在这些操作中需要的仪器:托盘天平、药匙、量筒、胶头滴管、烧杯和玻璃棒,故不需要用到的仪器是C.
(2)配制50克18%的食盐水,首先计算配制溶液所需食盐和水的质量,再称量所需的食盐和量取水,最后进行溶解.
(3)溶质质量=溶液质量×溶质的质量分数,配制50克18%的食盐水,需氯化钠的质量=50g×18%=9g;溶剂质量=溶液质量-溶质质量,则所需水的质量=50g-9g=41g(合41mL).
故答案为:(1)C;(2)计算;称量;溶解;(3)41.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤(计算、称量、溶解)、所需仪器等是正确解答本题的关键.

练习册系列答案
 每课必练系列答案
每课必练系列答案
相关题目
12.小萱和小屏分别进行酸碱中和实验,将0.5M氢氧化钠溶液装入滴定管中,开始滴入装有0.5M、3mL盐酸和数滴酚酞指示剂的锥形瓶内,且不时摇晃锥形瓶,直到溶液颜色发生变化为止.表为过程中,氢氧化钠溶液用量的刻度和锥形瓶内溶液颜色的记录,关于二人用量不同的结果,下列叙述何者正确?( )
小萱
小屏
小萱
| NaOH(mL) | 锥形瓶内溶液颜色 |
| 0 | 无色 |
| 0.2 | 无色 |
| 0.5 | 无色 |
| 1.0 | 无色 |
| 1.5 | 无色 |
| 2.0 | 无色 |
| 4.0 | 红色 |
| NaOH(mL) | 锥形瓶内溶液颜色 |
| 0 | 无色 |
| 1.0 | 无色 |
| 2.0 | 无色 |
| 2.5 | 无色 |
| 2.7 | 无色 |
| 2.9 | 无色 |
| 3.1 | 红色 |
| A. | 小萱的结果较准确,瓶内溶液变红色代表此时溶液呈碱性 | |
| B. | 小屏的结果较准确,瓶内溶液变红色代表此时溶液呈碱性 | |
| C. | 小萱的结果较准确,接近变色范围时应逐次增加氢氧化钠滴入量 | |
| D. | 小屏的结果较准确,接近变色范围时应逐次减少氢氧化钠滴入量 |
9.将一杯质量分数为22%的盐水倒去一半后,剩下的盐水质量分数为( )
| A. | 11% | B. | 22% | C. | 44% | D. | 不一定 |
16.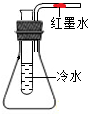 如图所示,导管内有一段红墨水,试管中盛有适量的冷水,容器的气密性良好.现往试管中加入下列某种物质,红墨水不会移动的是( )
如图所示,导管内有一段红墨水,试管中盛有适量的冷水,容器的气密性良好.现往试管中加入下列某种物质,红墨水不会移动的是( )
 如图所示,导管内有一段红墨水,试管中盛有适量的冷水,容器的气密性良好.现往试管中加入下列某种物质,红墨水不会移动的是( )
如图所示,导管内有一段红墨水,试管中盛有适量的冷水,容器的气密性良好.现往试管中加入下列某种物质,红墨水不会移动的是( )| A. | 氢氧化钠固体 | B. | 生石灰 | C. | 浓硫酸 | D. | 蔗糖 |
6.实验室有以下两种途径制取铜:
(1)CuO$\stackrel{H_{2}SO_{4}}{→}$CuSO4$\stackrel{Zn}{→}$Cu(2)Zn $\stackrel{H_{2}SO_{4}}{→}$H2$\stackrel{CuO}{→}$Cu
假设每步反应都完全,要制得等质量的铜,两个途径相比较,下列有关说法中正确的是( )
(1)CuO$\stackrel{H_{2}SO_{4}}{→}$CuSO4$\stackrel{Zn}{→}$Cu(2)Zn $\stackrel{H_{2}SO_{4}}{→}$H2$\stackrel{CuO}{→}$Cu
假设每步反应都完全,要制得等质量的铜,两个途径相比较,下列有关说法中正确的是( )
| A. | 消耗等质量的H2SO4 | B. | 消耗等质量的CuO | ||
| C. | 生成等质量的ZnSO4 | D. | 所有反应的类型都相同 |
13.下列有关盐酸叙述错误的是( )
| A. | 打开盛有浓盐酸的试剂瓶瓶塞,在瓶口出现白雾 | |
| B. | 稀盐酸可用于除铁锈 | |
| C. | 浓盐酸可用来干燥氧气 | |
| D. | 在稀盐酸滴加氢氧化钡溶液,出现白色沉淀 |
10.氢氧化钠可作干燥剂,但不能用它干燥的气体是:①CO ②CO2③H2④SO2⑤O2 ⑥H2S( )
| A. | ①② | B. | ③④ | C. | ④⑤⑥ | D. | ②④⑥ |