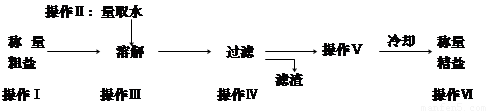题目内容
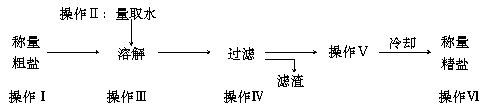
粗盐中含有可溶性杂质(氯化镁、氯化钙等)和不溶性杂质.粗盐提纯的操作步骤如下.
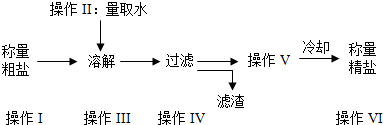
①上述过程中除去的杂质是 ;
②操作Ⅰ的目的是:a ;b.计算产率;
③量取水需要用到的仪器是 ;
④操作Ⅴ是 .

①上述过程中除去的杂质是
②操作Ⅰ的目的是:a
③量取水需要用到的仪器是
④操作Ⅴ是
分析:过滤可以除去不溶于水的杂质;
根据粗盐的质量可以判断需要水的质量;
用量筒和胶头滴管可以量取一定体积的水;
蒸发滤液可以得到固体物质.
根据粗盐的质量可以判断需要水的质量;
用量筒和胶头滴管可以量取一定体积的水;
蒸发滤液可以得到固体物质.
解答:解:①上述过程中能够除去粗盐中的不溶性杂质,而氯化镁和氯化钙不能除去.
故填:除去粗盐中的不溶性杂质.
②称量出粗盐的质量后,可以计算需要水的质量.
故填:计算需水量.
③量取水时,当量筒中的水接近需要的刻度时,应该改用胶头滴管滴加,以免水过量.
故填:量筒和胶头滴管.
④蒸发滤液可以得到精盐.
故填:蒸发.
故填:除去粗盐中的不溶性杂质.
②称量出粗盐的质量后,可以计算需要水的质量.
故填:计算需水量.
③量取水时,当量筒中的水接近需要的刻度时,应该改用胶头滴管滴加,以免水过量.
故填:量筒和胶头滴管.
④蒸发滤液可以得到精盐.
故填:蒸发.
点评:实验过程中,只能够除去不溶于水的杂质,不能除去氯化镁、氯化钙,因为氯化镁、氯化钙易溶于水,通过上述操作不能除去.

练习册系列答案
相关题目
某课外活动小组从海边盐滩上获得了一定量的粗盐,欲进行粗盐提纯的探究活动.请你参与其中,完成探究活动中的有关问题.
(1)查阅资料
①粗盐中含有较多的可溶性杂质(MgCl2、CaCl2等)和不溶性杂质(泥沙等).
②氯化钠在室温(20℃)时的溶解度为36.0g.
③Mg2+、Ca2+的碱和盐的溶解性(20℃)如下表:
说明:“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水.
(2)实验方案设计与问题讨论
①溶解(20℃)用托盘天平称取10.0g粗盐,用药匙将该粗盐逐渐加入到盛有10mL水的烧杯里,边加边搅拌,直到粗盐不再溶解为止.此时加入的粗盐质量至少是 g.
②除杂若要除去粗盐中的可溶性杂质CaCl2,可向其中加入过量的Na2CO3溶液;若要除去杂质MgCl2,可向其中加入过量的 溶液,然后按右图所示装置进行 操作.再向滤液中加入适量的 即得到氯化钠溶液.如果观察所得滤液是浑浊的,再过滤,仍浑浊,其可能的原因是: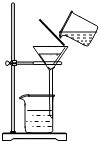 .
.
③蒸发
(3)实践实验操作过程略.
(1)查阅资料
①粗盐中含有较多的可溶性杂质(MgCl2、CaCl2等)和不溶性杂质(泥沙等).
②氯化钠在室温(20℃)时的溶解度为36.0g.
③Mg2+、Ca2+的碱和盐的溶解性(20℃)如下表:
| 阳离子\阴离子 | OH- | NO3- | SO42- | CO32- |
| Mg2+ | 不 | 溶 | 溶 | 微 |
| Ca2+ | 微 | 溶 | 微 | 不 |
(2)实验方案设计与问题讨论
①溶解(20℃)用托盘天平称取10.0g粗盐,用药匙将该粗盐逐渐加入到盛有10mL水的烧杯里,边加边搅拌,直到粗盐不再溶解为止.此时加入的粗盐质量至少是
②除杂若要除去粗盐中的可溶性杂质CaCl2,可向其中加入过量的Na2CO3溶液;若要除去杂质MgCl2,可向其中加入过量的

③蒸发
(3)实践实验操作过程略.