题目内容
为了测定液化气中丙烷(C3H8)在氧气不足时的燃烧产物,将一定量的丙烷和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
| 物质 | 丙烷 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 4.4 | 12.8 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
下列判断正确的是( )
|
| A. | 表中a的值为5.6 | B. | X可能是该反应的催化剂 |
|
| C. | X可能含有氢元素 | D. | X只含碳元素 |
| 质量守恒定律及其应用;催化剂的特点与催化作用.. | |
| 专题: | 化学用语和质量守恒定律. |
| 分析: | A、根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,则可求出a的质量; B、X在反应前质量为0,而反应后质量为5.6克,则不符合催化剂的特点“只改变反应速率,而本身的质量和化学性质都不变”,故X一定不是该反应的催化剂; C、根据质量守恒定律,反应前后元素的质量不变,可求4.4克丙烷(C3H8)中氢元素的质量,再求水中氢元素的质量,二者比较,再作结论; D、根据化学方程式计算,可求:4.4克丙烷(C3H8)中碳、氢元素的质量,推测是否含有氧元素. |
| 解答: | 解: A、根据质量守恒定律,反应前后质量相等,故4.4g+12.8g=7.2g+4.4g+a,则a=5.6g,故A正确; B、X在反应前质量为0,而反应后质量为5.6克,则不符合催化剂的特点“一变二不变”,故X一定不是该反应的催化剂,故B错误; C、根据质量守恒定律,化学反应前后各元素的质量不变:可求4.4克丙烷(C3H8)中氢元素的质量为:4.4g××100%=0.8克,水中氢元素的质量为:×100%×7.2g=0.8克,显然二者相等,则说明X中一定不含有氢元素了,故C错误; D、水中氢元素的质量为:×100%×7.2g=0.8克,而二氧化碳中碳元素的质量为4.4g××100%=1.2克,而4.4克丙烷(C3H8)中碳、氢元素的质量分别为:4.4g××100%=3.6克,4.4g××100%=0.8克,故X中一定含有碳元素3.6g﹣1.2g=2.4g<5.6克,故X还含有氧元素,故D错误. 故选:A. |
| 点评: | 本题主要考查学生运用质量守恒定律进行推断的能力;掌握根据化学方程式计算的方法. |

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案下列关于物质的性质叙述中属于化学性质的是( )
|
| A. | 炭黑黑色 | B. | 磁铁磁性 | C. | 面粉可燃 | D. | 铜能导电 |
下列关于金属的说法正确的是( )
|
| A. | 通过高炉炼得的铁为纯铁 |
|
| B. | 人类使用金属铝的年代早于铜、铁 |
|
| C. | 武德合金的熔点高,可用于制造保险丝 |
|
| D. | “真金不怕火炼”表明金在高温条件下也很难与氧气反应 |
除去下列物质中的少量杂质(括号内为杂质),所用试剂和操作正确的是( )
| 选项 | 物质 | 选用试剂及操作 |
| A | N2(O2) | 将气体通过灼热的木炭粉 |
| B | 锌粉(铁粉) | 用磁铁吸引 |
| C | CuO(Cu) | 在空气中加热 |
| D | CuSO4溶液(H2SO4) | 加入足量的铜粉,过滤 |
|
| A. | A | B. | B | C. | C | D. | D |
下表为家庭中一些常见物质的pH。
| 物质 | 食醋 | 牙膏 | 食盐水 | 肥皂水 | 酱油 |
| pH | 2~3 | 8~9 | 7 | 10 | 4~5 |
蚊子、蜂等昆虫叮咬人时,会向人体射入一种酸性物质,使人的皮肤红肿、瘙痒、疼痛,要消除这种症状,可在叮咬处涂抹下列物质中的( )
A.牙膏或肥皂水 B.食盐水
C.酱油 D.食醋
 ③木炭具有还原性,可以冶炼金属。请在 内填入配平后的系数。
③木炭具有还原性,可以冶炼金属。请在 内填入配平后的系数。

 (8) Fe3O4+ C
(8) Fe3O4+ C Fe+ CO2↑
Fe+ CO2↑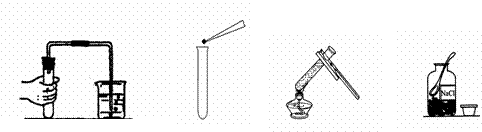 下列实验操作正确的是:( )
下列实验操作正确的是:( )