题目内容
7.有浓硫酸、烧碱、大理石、金刚石、氢氧化铝、一氧化碳六种物质,请选择这些物质的化学式填空:(1)用作建筑材料的是CaCO3;
(2)用于切割玻璃的是C;
(3)用于干燥二氧化碳的是H2SO4;
(4)引起煤气中毒的是CO;
(5)露置在空气中容易吸收二氧化碳而变质的是NaOH;
(6)可用于治疗胃酸过多的是Al(OH)3.
分析 首先根据题意确定物质的化学名称,然后根据书写化学式的方法和步骤写出物质的化学式即可.
解答 解:(1)大理石是一种常用的建筑材料,其主要成分是碳酸钙,故填:CaCO3;
(2)金刚石是硬度最大的矿物之一,常用于切割玻璃,故填:C;
(3)浓硫酸具有吸水性,可用来干燥二氧化碳气体,故填:H2SO4;
(4)一氧化碳俗称煤气,是一种有毒气体,故填:CO;
(5)烧碱是氢氧化钠的俗称,能吸收空气中的二氧化碳而发生变质,故填:NaOH;
(6)氢氧化铝是一种碱,能与胃酸中的盐酸发生中和反应,可用于治疗胃酸过多,故填:Al(OH)3.
点评 本题难度不大,熟练掌握常见物质的性质、用途、组成及化学式的书写是正确解答此类题的关键所在.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
相关题目
18.下列说法中正确的是( )
| A. | 原子是由原子核和核外电子构成的 | B. | 分子是保持物质性质的微粒 | ||
| C. | 原子是不能再分的微粒 | D. | 离子不一定带有电荷 |
15.物理、化学为人类生活和社会发展起到了巨大的推进作用.对下列四个主题下的知识归纳都正确的一组是( )
| A生活常识 | B物质鉴别 |
| 菜刀刀刃很薄--增大压强 “餐具洗”去油污--乳化作用 | 食盐与亚硝酸钠--品尝 尿素与硫酸铵--加熟石灰研磨闻气味 |
| C安全常识 | D环境保护 |
| 发生触电事故--首先切断电源 厨房燃气泄漏--迅速打开排风扇 | 减少白色污染--开发利用新能源 减少水污染--不使用化肥和农药 |
| A. | A | B. | B | C. | C | D. | D |
2.如图所示基本实验操作中,正确的是( )
| A. | 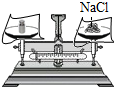 称取氯化钠固体 | B. | 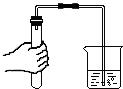 检验装置气密性 | C. |  稀释浓硫酸 | D. | 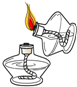 点燃酒精灯 |
19.请你参与某学习小组进行研究性学习的过程,并协助完成相关任务.
【研究课题】探究热水壶底部水垢的主要成分
【查阅资料】该小组同学通过查阅资料知道,天然水中一般都含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐、碱等的混合物).同时,他们还查阅到下列有关物质的溶解性:
【提出猜想】水垢的主要成分一定含有和,可能含有Ca(OH)2和MgCO3.
【设计方案】(1)甲同学在烧杯中放入少量研碎的水垢,加入适量蒸馏水充分搅拌,取上层清液加入,没有白色沉淀,说明水垢中无Ca(OH)2.
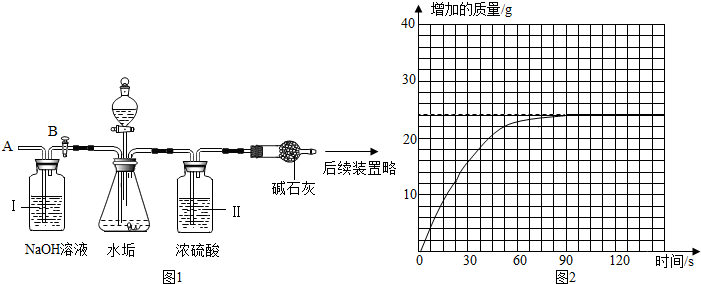
(2)乙同学设计了下列实验装置,进一步确定水垢中含有碳酸盐的成分.其主要实验步骤如下:
①按图组装仪器,将50g水垢试样放入锥形瓶中,加入足量盐酸溶液;
②测量一定时间内干燥管内物质增加的质量(见图2曲线);
③待锥形瓶中不再产生气泡时,打开活塞B,从导管A处缓缓鼓入一定量的空气;
④再次称量干燥管内物质增加的质量;
⑤重复③和④的操作,直至干燥管内物质质量不变
讨论:
a.步骤①加入样品前还应装置的气密性检查.
b.装置Ⅱ的作用是吸收CO2中的水;从导管A处缓缓鼓入一定量的空气时,装置Ⅰ的作用是除去空气中的CO2.
c.研究性小组的同学通过简单计算,认为水垢中一定含有MgCO3,理由是即使50g水垢全部为CaCO3,产生CO2的质量应为22g,而实验测得生成的CO2质量>22g.
【实验结论】通过上述探究可知:水垢的主要成分有Mg(OH)2、CaCO3、MgCO3.
【研究课题】探究热水壶底部水垢的主要成分
【查阅资料】该小组同学通过查阅资料知道,天然水中一般都含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐、碱等的混合物).同时,他们还查阅到下列有关物质的溶解性:
| 物质 | Ca(HCO3)2 | Mg(HCO3)2 | Ca(OH)2 | Mg(OH)2 | CaCO3 | MgCO3 |
| 溶解性 | 可溶 | 可溶 | 微溶 | 不溶 | 不溶 | 微溶 |
【设计方案】(1)甲同学在烧杯中放入少量研碎的水垢,加入适量蒸馏水充分搅拌,取上层清液加入,没有白色沉淀,说明水垢中无Ca(OH)2.
(2)乙同学设计了下列实验装置,进一步确定水垢中含有碳酸盐的成分.其主要实验步骤如下:
①按图组装仪器,将50g水垢试样放入锥形瓶中,加入足量盐酸溶液;
②测量一定时间内干燥管内物质增加的质量(见图2曲线);
③待锥形瓶中不再产生气泡时,打开活塞B,从导管A处缓缓鼓入一定量的空气;
④再次称量干燥管内物质增加的质量;
⑤重复③和④的操作,直至干燥管内物质质量不变

讨论:
a.步骤①加入样品前还应装置的气密性检查.
b.装置Ⅱ的作用是吸收CO2中的水;从导管A处缓缓鼓入一定量的空气时,装置Ⅰ的作用是除去空气中的CO2.
c.研究性小组的同学通过简单计算,认为水垢中一定含有MgCO3,理由是即使50g水垢全部为CaCO3,产生CO2的质量应为22g,而实验测得生成的CO2质量>22g.
【实验结论】通过上述探究可知:水垢的主要成分有Mg(OH)2、CaCO3、MgCO3.
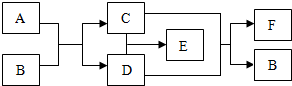 物质A已被世界卫生组织确定为致癌和致畸性物质.新装修的房子里,常常因为该物质超标而充斥着刺眼、刺鼻的异味,其溶液还可用于浸制动物标本.在A~F六种物质中,B、C为气体,D是生活中常见的液体,F为营养物质,且它们之间在一定条件下的转化关系如图所示,请依此回答问题.
物质A已被世界卫生组织确定为致癌和致畸性物质.新装修的房子里,常常因为该物质超标而充斥着刺眼、刺鼻的异味,其溶液还可用于浸制动物标本.在A~F六种物质中,B、C为气体,D是生活中常见的液体,F为营养物质,且它们之间在一定条件下的转化关系如图所示,请依此回答问题.