题目内容
19. 水与人类生活和生产密切相关.
水与人类生活和生产密切相关.(1)自来水属于混合物(填“纯净物”或“混合物”).
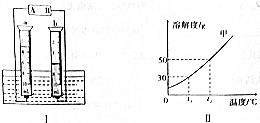
(2)通过太阳能电池电解水获取氢能是绿色能源发展的方向.如图Ⅰ所示,写出电解水的化学方程式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;电解水的实验中,加入适量的NaOH可以增加水的导电性而使电解速率加快,NaOH可以增加水导电的原因是氢氧化钠在水中会电离出能够自由移动的钠离子和氢氧根离子.
(3)0.9%的生理盐水中质量分数最大的元素是氧.
(4)如图Ⅱ是甲物质的溶解度曲线图,据图回答:
①t1℃,要完全溶解15g甲物质至少需要水50g.
②t2℃甲物质饱和溶液中溶质的质量分数是33.3%.
分析 (1)混合物是由多种物质组成的物质;纯净物是只有一种物质组成;
(2)根据电解水的原理以及氢氧化钠的电离来分析;
(3)根据溶液的组成以及元素的质量比来分析;
(4)根据溶解度曲线的意义来分析.
解答 解:(1)自来水是由水、氯化钙等多种物质组成的物质,属于混合物,故填:混合物;
(2)水在通电的条件下生成氢气和氧气;氢氧化钠在水中会电离出能够自由移动的钠离子和氢氧根离子,增强了水的导电性;故填:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;氢氧化钠在水中会电离出能够自由移动的钠离子和氢氧根离子;
(3)0.9%的生理盐水中水的含量最大,水中氢元素与氧元素的质量比为1:8,可见氧元素的质量分数最大;故填:氧;
(4)由溶解度曲线可知,t1℃,甲的溶解度为30g,也就是在该温度下的100g水中最多溶解30g甲,则溶解15g甲物质,至少需要50g水;t2℃甲物质的溶解度为50g,所以该温度下的饱和溶液中溶质的质量分数是$\frac{50g}{50g+100g}×100%≈33.3%$;故填:①50;②33.3%.
点评 本题考查了学生对溶解度曲线的认识和简单应用,难度不大.

练习册系列答案
相关题目
12.下列实验现象的描述,不正确的是( )
| A. | 铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| B. | 硫在氧气中燃烧,发出蓝紫色火焰 | |
| C. | 红磷在空气中燃烧,产生大量的白烟 | |
| D. | 氢气在空气中燃烧,生成有刺激性气味的气体 |
7.化学学习中,对比、归纳、整理是一种重要的学习过程.请完成如表
| 构成物质的三种微粒 | 分子、原子、离子 |
| 酒精灯的三层火焰 | 外焰、内焰、焰心 |
| 自然界的三大化石燃料 | 煤、石油、天然气 |
14.下列说法正确的是( )
| A. | 铵态氮肥与草木灰混合使用可以明显提高肥效 | |
| B. | 合金的硬度一般比各成分金属小 | |
| C. | 用灯帽盖灭酒精灯,是为了降低可燃物的温度 | |
| D. | 金刚石与石墨的物理性质不同,构成物质的原子排列方式不同 |
4.规范的实验操作是获得实验成功的重要保证,如图实验操作错误的是( )
| A. | 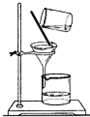 过滤 | B. | 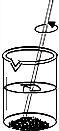 溶解 | C. | 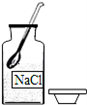 取固体药品 | D. |  蒸发 |
11.下列元素和人体健康的关系,对应错误的是( )
| A. | 缺钙会导致侏儒症 | |
| B. | 缺铁会导致贫血 | |
| C. | 缺锌会导致儿童发育停滞,智力低下 | |
| D. | 碘摄入过量会导致甲状腺疾病 |
8.小明阅读《科学画报》后,对抽烟的爸爸说:“吸烟有害健康,我和妈妈都在被动吸烟”小明这样说的主要原因是( )
| A. | 分子很小 | B. | 分子间有间隙 | C. | 分子不停运动 | D. | 分子间有作用力 |
 学习二氧化碳的性质和制取知识后,明明同学想探究鸡蛋壳的主要成分,他利用家庭中现有用品做如下实验:
学习二氧化碳的性质和制取知识后,明明同学想探究鸡蛋壳的主要成分,他利用家庭中现有用品做如下实验: