题目内容
19.请根据图1所示的实验室中实验装置图填空.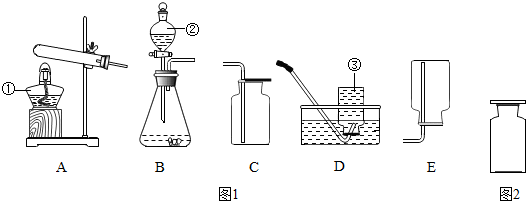
(1)完成图中标有数字的仪器的名称:①酒精灯,②长颈漏斗,③集气瓶.
(2)实验室制取二氧化碳的发生装置和收集装置分别是B和C(填字母编号),反应的化学方程式是:CaCO3+2HCl=CaCl2+CO2↑+H2O.
(3)为什么长期盛放石灰水的试剂瓶壁上会出现白膜,它是CaCO3(填化学式),形成这种白色固体的原因是(用化学方程式表示)Ca(OH)2+CO2═CaCO3↓+H2O.
(4)图2是已收集满的一瓶无色无毒的纯净气体.请你用学过的知识进行探究,确定该气体可能是什么气体,填写下表.(写一种可能)
| 假设 | 验证方法及操作 | 现象及结论 |
分析 (1)要熟悉各种仪器的名称、用途和使用方法;
(2)根据发生装置的选择要看反应物的状态和反应条件;收集装置的选择要看气体的密度和溶解性;实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳,书写化学方程式;
(3)根据已有的知识进行分析,二氧化碳能与澄清石灰水反应生成不溶于水的碳酸钙;
(4)密度大于空气的气体在存放时,集气瓶正放,如本题中的存放方式;气体密度小于空气时,存放气体的集气瓶应倒放;验证氧气,用带火星的木条进行,看到木条复燃,则气体可确定为氧气.
解答 解:(1)图中标有数字的仪器的名称:①酒精灯;②长颈漏斗;③集气瓶.
(2)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,故发生装置的选B;二氧化碳能够溶于水,不能用排水法收集,密度比空气大,可以用向上排空气法收集,即用C装置收集.
大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳,故反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)由于氢氧化钙溶液易和空气中的二氧化碳反应生成碳酸钙和水,因此久置空气的石灰水瓶壁上就会有一层白色固体,这层白色固体就是碳酸钙,而碳酸钙不溶水,故答案为:CaCO3,Ca(OH)2+CO2═CaCO3↓+H2O;
(4)若该瓶气体可能是氧气,可以使用带火星的木条伸进瓶内,观察木条是否复燃
| 假设 | 验证方法及操作 | 现象结论 |
| 可能是氧气 | 将带火星的木条伸进集气瓶内,观察到木条是否复燃 | 木条复燃该气体为氧气 |
(1)①酒精灯,②长颈漏斗,③集气瓶;(2)B,C; CaCO3+2HCl=CaCl2+CO2↑+H2O;
(3)CaCO3,Ca(OH)2+CO2═CaCO3↓+H2O;(4)
| 假设 | 验证方法及操作 | 现象结论 |
| 可能是氧气 | 将带火星的木条伸进集气瓶内,观察到木条是否复燃 | 木条复燃该气体为氧气 |
点评 本题主要考查仪器的用途、化学方程式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素.

| A. | 原子质量小,分子质量大 | |
| B. | 原子体积小,分子体积大 | |
| C. | 在化学变化中,分子能分,而原子不能再分 | |
| D. | 分子能保持物质的化学性质,而原子不能 |
| A. | CuO | B. | Al2O3 | C. | CaO | D. | ZnO |
| 物质 | 杂质 | 除杂质应选用的试剂和操作方法 | |
| A | CO2 | CO | 通入O2,点燃 |
| B | 铁粉 | 铜粉 | 加入适量的稀盐酸,过滤 |
| C | Cu(NO3)2溶液 | AgNO3溶液 | 加入过量的铜粉,过滤 |
| D | NaOH固体 | Na2CO3固体 | 加入过量盐酸,蒸发 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 浓硫酸暴露在空气中,溶液的质量会变大 | |
| B. | 铝丝表面形成致密的保护膜 | |
| C. | 浓盐酸敞口放置,溶质的质量分数会变小 | |
| D. | 生石灰暴露在空气中会变质 |
| A. | 55 | B. | Mn | C. | 23 | D. | Na |
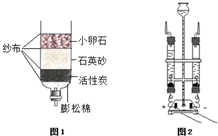 水是生命之源.
水是生命之源.