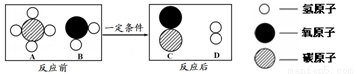
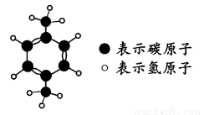
题目内容
(8分)在学校的元旦联欢会上,某同学表演了“水能生火”的魔术。他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来。小明很感兴趣,于是,他和同学们进行探究。
【提出问题】过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
【猜想】①可能有一种气体和另一种物质生成;
②反应过程中可能有能量变化。
【设计装置】如图所示
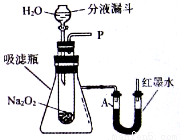
【实验探究】实验一:探究反应后生成的气体是什么?
(1)小利猜想生成的气体可能是氢气,也可能是氧气。小利猜想的依据是 。
(2)小宁打开装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃。说明生成的气体是 。
(3)实验过程中,还观察到U型管A端红墨水液面下降,说明本反应是 反应(填“放热”或“吸热”反应)。
【资料】氢氧化钠与稀盐酸有反应但无明显现象,碳酸钠与稀盐酸反应有气体生成。
实验二:继续探究反应后生成的另一种物质是什么?
(1)小明认为反应生成了碳酸钠,小军认为不可能,应生成氢氧化钠,你认为这两位同学,谁的猜想是正确的____________。
(2)为了验证上述同学的想法是否正确,可以取出少量样品于试管中,然后加入________根据是否有___________________生成来判断。
(3)根据以上结论,写出过氧化钠和水反应的化学方程式: 。
实验一(1)化学反应前后元素种类不变(反应前有氢元素和氧元素)
(2)氧气(3)放热
实验二(1)小军 (2)稀盐酸 气泡 (3)2Na2O2 +2H2O =4NaOH +O2↑
【解析】
试题解析:实验一、燃烧需要可燃物,氧气,温度达到着火点。⑴、有质量守恒定律,化学反应中原子的种类数目不变,Na、O、H原子能构成的且与燃烧有关的气体分子只能是H2或者O2;⑵氧气纯度高燃烧越剧烈,空气中火星遇到该气体复燃,是氧气;⑶、温度升高分子间隙增大,瓶内气压增大把红墨水外排。
实验二、⑴化学反应遵守质量守恒定律,而反应物只含有Na、O、H,不含C;⑵碳酸钠含有碳酸根相对于氢氧化钠更易检测证明,碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,有气体生成;反应物为Na2O2和H2O,生成物是NaOH和O2,反应条件是常温
考点:由质量守恒定律和实验现象推测化学反应,由化学反应方程式推测现象。

下列除去杂质的方法中,不正确的是
序号 | 物质 | 杂质 | 除去杂质的方法 |
① | NaCl固体 | 泥沙 | 溶解、过滤、蒸发 |
② | C | CuO | 高温灼烧 |
③ | FeSO4溶液 | CuSO4 | 加入足量锌粒,充分反应,过滤 |
④ | CO2 | CO | 向混合气体中通氧气,点燃 |
A.①② B.③④ C.②③ D.②③④
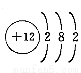 不能确定的是
不能确定的是