题目内容
3.通过化学课的学习,我们知道有许多途径可以制取氧气.如:A、分解过氧化氢 B、分离空气
C、加热高锰酸钾 D、加热氯酸钾和二氧化锰
(1)相信你在D处还可以写出另一种制取氧气的方法.
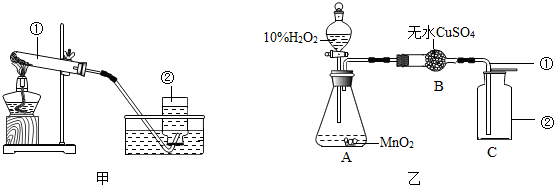
(2)写出标号仪器的名称①试管,②集气瓶.
(3)若用加热高锰酸钾的方法制取氧气,可选择如图装置甲(选填“甲”或“乙”),理由是KMnO4是固体,反应需要加热.该反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.实验过程中发现水槽中的水变成红色.可能的原因是试管口没有塞上一团棉花,停止加热时应先将导管移离水槽,然后再熄灭酒精灯.
(4)某化学兴趣小组的同学们用如图乙装置进行探究实验,请回答:
1)锥形瓶内装有二氧化锰和双氧水,请写出瓶中发生的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;反应中二氧化锰起催化作用.
2)白色的无水硫酸铜遇水蒸气会变蓝,有关的化学方程式为:
CuSO4(白)+5H2O→CuSO4•5H2O(蓝)
请预测本实验过程中,无水硫酸铜是否会变蓝?是(填“是”或“否”).装置B的作用是干燥气体.
3)图乙中的收集方法称为向上排空气法.图中导气管插入仪器C的位置是否正确?是(填“是”或“否”).将带火星的木条伸到集气瓶口,若木条复燃,则证明O2已收集满.
分析 (1)根据制取氧气的方法还有加热氯酸钾和二氧化锰混合或电解水物进行解答;
(2)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(3)根据高锰酸钾制取氧气的反应物是固体,反应条件是加热,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,试管口需要放一团棉花,防止高锰酸钾粉末进入导管,以及实验结束的正确操作进行分析;
(4)1)根据过氧化氢在二氧化锰的催化作用下生成水和氧气,二氧化锰是该反应的催化剂进行分析;
2)根据无水硫酸铜遇水显蓝色,浓硫酸有吸水性进行分析;
3)根据图乙中的收集方法称为向上排空气法,图中导气管插入仪器C的底部,氧气有助燃性进行分析.
解答 解:(1)制取氧气的方法还有加热氯酸钾和二氧化锰混合物或电解水;
(2)通过分析题中所指仪器的作用可知,①是试管,②是集气瓶;
(3)高锰酸钾制取氧气的反应物是固体,反应条件是加热,所以可选择如图装置甲,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,试管口需要放一团棉花,防止高锰酸钾粉末进入导管,停止加热时应先将导管移离水槽,然后再熄灭酒精灯;
(4)1)过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,二氧化锰是该反应的催化剂,起催化作用;
2)无水硫酸铜遇水显蓝色,浓硫酸有吸水性;
3)图乙中的收集方法称为向上排空气法,图中导气管插入仪器C的底部,氧气有助燃性,所以将带火星的木条伸到集气瓶口,若木条复燃,则证明氧气集满.
故答案为:(1)电解水(或加热氯酸钾和二氧化锰);
(2)试管,集气瓶;
(3)甲,KMnO4 是固体,反应需要加热,2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$ K2MnO4+MnO2+O2↑,试管口没有塞上一团棉花,将导管移离水槽,熄灭酒精灯;
(4)1)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,催化;
2)是,干燥气体;
3)向上排空气法,是,O2已收集满.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

 计算高手系列答案
计算高手系列答案| A. | 酸能使紫色石蕊试液变红,通入二氧化碳后的紫色石蕊试液变红,所以二氧化碳是酸 | |
| B. | 溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小 | |
| C. | 分子可以构成物质,所以物质一定是由分子构成的 | |
| D. | 增大氧气的浓度或增大可燃物与氧气的接触面积,都能促进可燃物燃烧,所以物质在氧气中燃烧比在空气中更剧烈 |
| A. | 打开浓盐酸的试剂瓶盖,瓶口会出现白雾 | |
| B. | 含硫火柴头燃烧产生的气体通入稀高锰酸钾溶液,溶液褪色 | |
| C. | 向加碘食盐溶液中滴加淀粉,溶液不变色 | |
| D. | 铁在空气中燃烧,火星四射,生成黑色固体 |
| 选项 | 待提纯的物质 | 选用的试剂 | 操作的方法 |
| A | CaCO3(CaCl2) | 水 | 溶解、过滤、结晶 |
| B | CaCl2溶液(HCl) | 过量CaCO3 | 过滤 |
| C | Cu(CuO) | 稀盐酸 | 溶解、过滤、洗涤、干燥 |
| D | CO2(CO) | 氧气 | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 属于有机化合物 | B. | 由两种金属和一种非金属组成 | ||
| C. | 铁元素的质量分数为33.73% | D. | 钠、铁、氧三种元素质量比是2:1:4 |
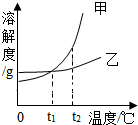 甲、乙两种物质的溶解度曲线如图所示,下列叙述正确的是( )
甲、乙两种物质的溶解度曲线如图所示,下列叙述正确的是( )| A. | 依据溶解度曲线可判断:甲的溶解度比乙的大 | |
| B. | 将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大 | |
| C. | 将t2℃时甲的饱和溶液变为不饱和溶液,可采取降温的方法 | |
| D. | t1℃时,甲和乙的饱和溶液各100g,其溶质的溶解度相等 |
| A. | 常用干燥剂:生石灰、烧碱、浓硫酸 | |
| B. | 混合物:煤、石油、冰水共存物 | |
| C. | 合成材料:合金、合成橡胶、合成纤维 | |
| D. | 复合肥料:尿素、硝酸钾、磷酸二氢铵 |
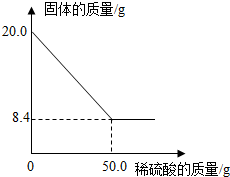 菱铁矿(主要成分是FeCO3)是炼铁的原料.现取20.0g菱铁矿,向其中加入足量稀硫酸,充分反应(菱铁矿中杂质不参加反应,且难溶于水),测得固体质量与所加稀硫酸的质量关系如图所示.请计算:
菱铁矿(主要成分是FeCO3)是炼铁的原料.现取20.0g菱铁矿,向其中加入足量稀硫酸,充分反应(菱铁矿中杂质不参加反应,且难溶于水),测得固体质量与所加稀硫酸的质量关系如图所示.请计算: