题目内容
11.海水是资源的宝库,海水淡化可获得淡水和浓海水.浓海水中主要离子的浓度如表:| 离子 | Na+ | Mg2+ | Cl- | SO${\;}_{4}^{2-}$ |
| 浓度/(g/L) | 63.7 | 28.8 | 144.6 | 46.4 |
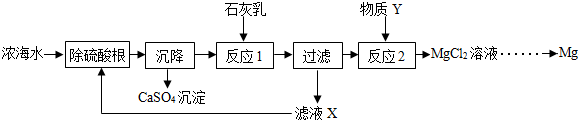
(1)补全由贝壳生产石灰乳的相应转化中所需的条件或反应物:贝壳$\stackrel{()}{→}$生石灰$\stackrel{()}{→}$石灰乳
(2)写出反应1的化学方程式:Ca(OH)2+MgCl2=CaCl2+Mg(OH)2↓.
(3)滤液X中溶质的主要成分有CaCl2、NaCl(填化学式).
(4)物质Y的名称是盐酸.
分析 (1)贝壳的主要成分是碳酸钙,高温煅烧生成氧化钙,氧化钙与水反应生成氢氧化钙;
(2)该反应是氢氧化钙与氯化镁的反应;
(3)该过程主要是分离氢氧化镁沉淀和溶液;
(4)将氢氧化镁这种碱转化为氯化镁这种盐,需要加入稀盐酸.
解答 解:(1)碳酸钙高温煅烧生成氧化钙,氧化钙与水反应生成氢氧化钙;故填:煅烧;水;
(2)反应1是氢氧化钙与氯化镁发生复分解反应生成氯化钙和氢氧化镁白色沉淀;故填:Ca(OH)2+MgCl2=CaCl2+Mg(OH)2↓;
(3)将物质过滤分离后所得溶液主要是氯化钙和氯化钠的溶液,故填:CaCl2、NaCl;
(4)酸碱中和生成盐和水,故加入的是稀盐酸,故填:盐酸;
点评 本题考查海水资源开发利用、有关计算等,是对基础知识的综合运用,需要学生具备扎实的基础,难度中等.

练习册系列答案
相关题目
2.下列图象能正确反映对应变化关系的是( )
| A. | 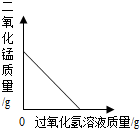 向一定量的二氧化锰中加入过氧化氢溶液 向一定量的二氧化锰中加入过氧化氢溶液 | |
| B. | 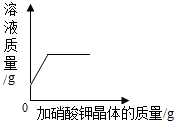 某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体 某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体 | |
| C. |  是将镁片和铁片(均足量)分别和等质量、等溶质质量分数的稀盐酸混合 是将镁片和铁片(均足量)分别和等质量、等溶质质量分数的稀盐酸混合 | |
| D. | 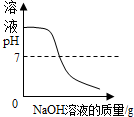 向一定量体积的稀盐酸中逐滴加入氢氧化钠溶液 向一定量体积的稀盐酸中逐滴加入氢氧化钠溶液 |
19.有甲、乙、丙、丁四瓶未知溶液,它们分别是Ca(OH)2、HCl、K2CO3、NaCl溶液中的一种.为了鉴别它们,各取少许溶液进行两两混合,实验记录如下:①甲+乙→有气泡产生;②甲+丙→有白色沉淀产生,由此可推断甲、乙、丙、丁依次为( )
| A. | K2CO3、Ca(OH)2、HCl、NaCl | B. | Ca(OH)2、HCl、NaCl、K2CO3 | ||
| C. | K2CO3、HCl、Ca(OH)2、NaCl | D. | K2CO3、NaCl、HCl、Ca(OH)2 |
6.现有X、Y、Z三种金属,只有Z在稀硫酸中无变化.如果把X放入Y的硫酸盐溶液中,X表面有Y析出.根据以上现象判断这三种金属的活动性由强到弱的顺序为( )
| A. | X、Y、Z | B. | X、Z、Y | C. | Z、X、Y | D. | Y、Z、X |
20.下列化学方程式与事实相符且正确的是( )
| A. | 碳在氧气中完全燃烧2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO | |
| B. | 用足量澄清石灰水检验二氧化碳:CO2+Ca(OH)2═CaCO3↓+H2O | |
| C. | 用稀盐酸除铁锈:2HCl+FeO═FeCl2+H2O | |
| D. | 用足量NaOH溶液在加热条件下检验NH4HCO3中NH4+:NaOH+NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+NaHCO3 |
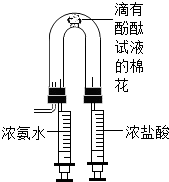 某兴趣小组设计了如图实验所示(夹持仪器略去).
某兴趣小组设计了如图实验所示(夹持仪器略去).
