题目内容
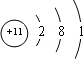
下列关于该元素的说法错误的是( )
| A.钠离子符号表示为Na |
| B.它的原子核外有11个电子 |
| C.它是一种金属元素 |
| D.它的阳离子含有11个质子 |
B、它的原子核外有2+8+1=11个电子,故选项正确;
C、钠是一种金属元素,故选项正确;
D、质子在原子核内,一般不会变化,所以它的阳离子含有11个质子,故选项正确.
故选A.

元素周期表是学习和研究化学的重要工具。请根据下表(元素周期表的部分内容)回答有关问题:
|
族 周期 |
I A |
II A |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
|
2 |
3 Li 锂 6.941 |
4 Be 铍 9.012 |
5 B 硼 10.81 |
6 C 碳 12.01 |
7 N 氮 14.01 |
8 O 氧 16.00 |
9 F 氟 19.00 |
10 Ne 氖 20.18 |
|
3 |
11 Na 钠 22.99 |
12 Mg 镁 24.31 |
13 Al 铝 26.98 |
14 Si 硅 28.09 |
15 P 磷 30.97 |
16 S 硫 32.06 |
17 Cl 氯 35.45 |
18 Ar 氩 39.95 |
(1)请从上表中查出关于硼元素的一条信息:_______________ ____________。
(2)不同元素的本质区别是 ( )
A.质子数 B.电子数 C.中子数 D.相对原子质量
(3)如图是钠原子的结构示意图,判断该原子容易 (填“得到”或“失去”)电子,钠离子的符号为

(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是 (填标号)。
a.C和Ne b.Be和Mg c.Al和Si d.F和Cl
(5)第9号氟元素和氢元素形成的化合物的水溶液氢氟酸(HF),可用于玻璃雕刻, 其主要原理是氢氟酸与玻璃的主要成分二氧化硅(SiO2)发生反应,生成四氟化硅气体(SiF4)和水(H2O,用化学式表示该反应 。
阅读下表中的数据,找一下有什么规律。
| 原子种类 | 原子核 | 核外电子数 | 1个原子的质量/kg | 相对原子质量 | |
| 质子数 | 中子数 | ||||
| 氢 | 1 | 0 | 1 | 1.674×10-27 | 1 |
| 碳 | 6 | 6 | 6 | 1.993×10―26 | 12 |
| 氧 | 8 | 8 | 8 | 2.657×10―26 | 16 |
| 钠 | 11 | 12 | 11 | 3.818×10―26 | 23 |
(1)由上表写出两条你获得的信息:________; ____________________。
(2)已知钠原子的结构示意图为 ,请问在化学反应中钠原子易______(填“得到”或“失去”)电子。
,请问在化学反应中钠原子易______(填“得到”或“失去”)电子。
(3)从上表四种元素中,选择适当的元素组成符合下列要求的物质,并用化学式填空:
①具有强烈腐蚀性的物质______;②人体中含量最多的物质______;③燃烧无污染,常作火箭发射燃料的物质______;④由上述四种元素组成的盐______。
| 原子种类 | 原子核 | 核外电子数 | 1个原子的质量/kg | 相对原子质量 | |
| 质子数 | 中子数 | ||||
| 氢 | 1 | 1 | 1.674×10-27 | 1 | |
| 碳 | 6 | 6 | 6 | 1.993×10-26 | 12 |
| 氧 | 8 | 8 | 8 | 2.657×10-26 | 16 |
| 钠 | 11 | 11 | 11 | 3.818×10-26 | 23 |
(2)已知钠原子的结构示意图
 ,请问在化学反应中钠原子易(填“得到”或“失去”)电子.
,请问在化学反应中钠原子易(填“得到”或“失去”)电子.(3)从上表四种元素中,选择适当的元素组成符合下列要求的物质,并用化学式填空:
①具有强烈腐蚀性的物质;
②人体中含量最多的物质;
③燃烧无污染,常作火箭发射燃料的物质;
④由上述四种元素组成的盐.

 ,请问在化学反应中钠原子易
,请问在化学反应中钠原子易

 ,请问在化学反应中钠原子易__(填“得到”或“失去”)电子。 (3)从上表四种元素中,选择适当的元素组成符合下列要求的物质,并用化学式填空:
,请问在化学反应中钠原子易__(填“得到”或“失去”)电子。 (3)从上表四种元素中,选择适当的元素组成符合下列要求的物质,并用化学式填空: