题目内容
 如图为KNO3、NaNO2(亚硝酸钠)、NaCl的溶解度曲线,请分析图象回答下列问题:
如图为KNO3、NaNO2(亚硝酸钠)、NaCl的溶解度曲线,请分析图象回答下列问题:①
②NaNO2属于
③NaNO2因外观与NaCl相似,经常会出现误食中毒的事件.20℃时,取这两种固体50g,分别加入到100g水中充分搅拌,没有溶解完的固体是
④若KNO3中混有少量的NaCl,可采用
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,物质的溶解性及影响溶解性的因素
专题:溶液、浊液与溶解度
分析:根据溶解度曲线可知物质的溶解度受温度的影响情况;交点表示该温度下两物质的溶解度相同;可以判断或比较相同温度下,不同物质溶解度的大小(或饱和溶液中溶质的质量分数的大小),以及溶液的状态.
解答:解:解:(1)KNO3与NaNO2的溶解度在60℃时交于一点,说明该温度下两物质的溶解度相同;故答案为:60;
(2)NaNO2在20℃时的溶解度大于10g,属于易溶物质,故填:易;
(3)观察溶解度曲线可知:20℃时NaNO2的溶解度大于NaCl的溶解度,且NaCl的溶解度小于50g,NaNO2的溶解度大于50g;所以20℃时,取两种固体各50g,分别加入到100g水中充分搅拌后,没有溶解完的固体是NaCl,NaNO2固体完全溶解依然不饱和;故答案为:NaCl;不饱和;
(4)硝酸钾的溶解度随温度升高变化明显,当KNO3中混有少量的NaCl,可采用降温结晶的方法,故填:降温结晶.
(2)NaNO2在20℃时的溶解度大于10g,属于易溶物质,故填:易;
(3)观察溶解度曲线可知:20℃时NaNO2的溶解度大于NaCl的溶解度,且NaCl的溶解度小于50g,NaNO2的溶解度大于50g;所以20℃时,取两种固体各50g,分别加入到100g水中充分搅拌后,没有溶解完的固体是NaCl,NaNO2固体完全溶解依然不饱和;故答案为:NaCl;不饱和;
(4)硝酸钾的溶解度随温度升高变化明显,当KNO3中混有少量的NaCl,可采用降温结晶的方法,故填:降温结晶.
点评:本题考查了溶解度曲线的应用,完成此题,可以依据溶解度曲线的意义进行.

练习册系列答案
相关题目
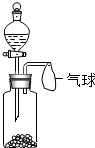 要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )
要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )①石灰石和稀盐酸 ②镁和稀盐酸
③氯化钠和水 ④生石灰和水.
| A、①②③④ | B、①②③ |
| C、①②④ | D、②③④ |
某工厂排放的酸性废水中含有较多的Cu2+,对农作物和人畜都有害,欲采用化学法除去有害成分,最好是加入下列物质中的( )
| A、食盐、硫酸 |
| B、胆矾、石灰水 |
| C、铁粉、生石灰 |
| D、苏打、盐酸 |
垃圾资源化的方法是( )
| A、填埋 | B、焚烧 |
| C、堆肥法 | D、分类回收法 |
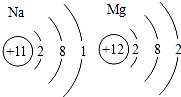 化学的学科特征是在原子、分子水平研究物质和创造物质.
化学的学科特征是在原子、分子水平研究物质和创造物质.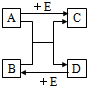 已知A、B、C、D、E是初中化学常见的物质,它们相互转化的关系如图所示.
已知A、B、C、D、E是初中化学常见的物质,它们相互转化的关系如图所示.