题目内容
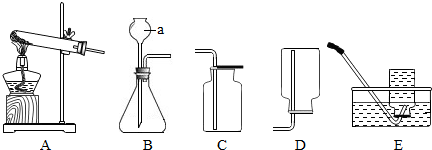
14. 如图是一种钙片标签的部分内容.根据标签内容完成下列填空:
如图是一种钙片标签的部分内容.根据标签内容完成下列填空:(1)碳酸钙中钙、碳、氧元素的质量比是10:3:12;
(2)碳酸钙中氧元素的质量分数是48%;
(3)每片钙片含碳酸钙的质量分数是75%;
(4)每片钙片含钙元素的质量是0.6g.
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据化合物元素的质量分数计算方法来分析;
(3)根据质量分数的计算方法来分析;
(4)根据化学式的意义及每片钙片的质量进行分析解答.
解答 解:(1)碳酸钙中钙、碳、氧三种元素的质量比为40:12:(16×3)=10:3:12.故填:10:3:12;
(2)碳酸钙中氧元素的质量分数是$\frac{16×3}{40+12+16×3}×100%$=48%,故填:48%;
(3)每片钙片含碳酸钙的质量分数是$\frac{1.5g}{2g}×100%$=75%,故填:75%;
(4)每片钙片含钙元素的质量是1.5g×$\frac{40}{40+12+16×3}×100%$=0.6g,故填:0.6g.
点评 本题难度不大,以标签上的文字说明为情景素材,考查了有关化学式、化学方程式的计算,培养了学生的灵活运用所学知识进行分析问题、解决问题的能力.

练习册系列答案
相关题目
4.下列应用和相应原理(用化学方程式表示)及基本反应类型都正确的是( )
| A. | 用石灰水检验二氧化碳:CO2+Ca(OH)2═CaCO3↓+H2O 复分解反应 | |
| B. | 比较铜和银的金属活动性:Cu+2AgCl═2Ag+CuCl2置换反应 | |
| C. | 铝制品有很好的抗腐蚀性:4Al+3O2═2Al2O3 化合反应 | |
| D. | 工业上制氧气:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ 分解反应 |
5.下列能源中,不会对环境造成污染且取之不尽的天然能源是( )
| A. | 氢气 | B. | 太阳能 | C. | 天然气 | D. | 可燃冰 |
9.下列各种物质中,氯元素化合价最高的是( )
| A. | NaClO4 | B. | HCl | C. | Cl2 | D. | ClO2 |
6.下列实验操作中,正确的是( )
| A. |  称取氯化钠 | B. | 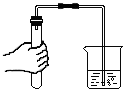 检查装置的气密性 | ||
| C. | 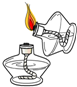 点燃酒精灯 | D. |  读取量筒的读数 |
3.下列物质中属于复合肥料的是( )
| A. | KNO3 | B. | NH4HCO3 | C. | Ca(H2PO4)2 | D. | CO(NH2)2 |
10.打开盛有下列各组物质的试剂瓶塞,在瓶口上方能看到白雾的一组是( )
| A. | 浓盐酸和食盐水 | B. | 浓硫酸和石灰水 | ||
| C. | 液氧和浓盐酸 | D. | 液氧和氢氧化钠的浓溶液 |