题目内容
11.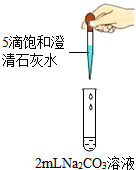 学习酸碱盐知识后,同学们知道碳酸钠溶液与氢氧化钙溶液能发生反应,可观察到溶液变浑浊.甲组同学进行如图1所示的实验,却未观察到预期现象.
学习酸碱盐知识后,同学们知道碳酸钠溶液与氢氧化钙溶液能发生反应,可观察到溶液变浑浊.甲组同学进行如图1所示的实验,却未观察到预期现象.【提出问题】未观察到浑浊的原因是什么?
【猜想和假设】
①与氢氧化钙溶液的浓度有关.若使用更大浓度的氢氧化钙溶液,会迅速产生浑浊.
②与碳酸钠溶液的浓度有关.若使用更大浓度的碳酸钠溶液,会迅速产生浑浊.
经讨论,同学们认为猜想①不合理,其理由是饱和石灰水已是该温度下质量分数最大的溶液.
【进行实验】乙组同学针对猜想②进行实验.
| 实验目的 | 实验操作 | 实验现象 | |
| 探究猜想② | 取4支试管,向其中分别加入… | 碳酸钠溶液浓度/% | 是否浑浊 |
| 10 | 不浑浊 | ||
| 5 | 不浑浊 | ||
| 1 | 浑浊 | ||
| 0.5 | 浑浊 | ||
(1)补全上述实验操作:取4支试管,向其中分别加入2mL浓度为10%、5%、1%、0.5%的碳酸钠溶液,再分别滴加5滴饱和石灰水.
(2)氢氧化钙溶液与碳酸钠溶液混合出现浑浊的化学方程式是Ca(OH)2+Na2CO3CaCO3↓+2NaOH.
(3)乙组实验证明:猜想②不成立,碳酸钠溶液浓度在0.5~10%的范围内,能否出现浑浊与碳酸钠溶液的浓度有关,其关系是碳酸钠溶液浓度大,不易产生浑浊.
【实验反思】
(1)丙组同学对乙组所做实验中未出现浑浊的原因进行探究.设计了多组实验,其中部分同学的实验过程及结果如图2

丙组同学的实验目的是探究碳酸钙能否溶解在碳酸钠溶液中.
(2)依据乙、丙两组的实验探究,丁组同学仍使用甲组的仪器和药品对甲组实验进行了改进,当滴入几滴某溶液后,溶液迅速变浑浊.其实验操作是取2mL饱和石灰水于试管中,滴加碳酸钠溶液.
分析 【猜想和假设】根据饱和石灰水已是该温度下质量分数最大的溶液解答;
【解释与结论】
(1)根据图示分析解答;
(2)根据氢氧化钙溶液与碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠解答;
(3)根据碳酸钠溶液浓度大,不易产生浑浊解答;
【实验反思】
(1)根据图示分析丙组同学的实验目的是探究碳酸钙能否溶解在碳酸钠溶液中解答;
(2)根据氢氧化钙溶液与碳酸钠溶液反应解答.
解答 解:
【猜想和假设】与氢氧化钙溶液的浓度有关.若使用更大浓度的氢氧化钙溶液,会迅速产生浑浊,猜想错误,因为饱和石灰水已是该温度下质量分数最大的溶液;
【解释与结论】
(1)根据图示和表格可知:取4支试管,向其中分别加入2 mL浓度为10%、5%、1%、0.5%的碳酸钠溶液,再分别滴加5滴饱和石灰水;
(2)氢氧化钙溶液与碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式是:Ca(OH)2+Na2CO3CaCO3↓+2NaOH;
(3)乙组实验证明:猜想②不成立,碳酸钠溶液浓度在0.5~10%的范围内,能否出现浑浊与碳酸钠溶液的浓度有关,其关系是碳酸钠溶液浓度大,不易产生浑浊;
【实验反思】
(1)根据图示分析丙组同学的实验目的是探究碳酸钙能否溶解在碳酸钠溶液中
(2)依据乙、丙两组的实验探究,丁组同学仍使用甲组的仪器和药品对甲组实验进行了改进,当滴入几滴某溶液后,溶液迅速变浑浊.其实验操作是取2 mL饱和石灰水于试管中,滴加碳酸钠溶液.
答案:
[猜想与假设]饱和石灰水已是该温度下质量分数最大的溶液;
[解释与结论](1)2 mL浓度为10%、5%、1%、0.5%的碳酸钠溶液,再分别滴加5滴饱和石灰水;
(2)Ca(OH)2+Na2CO3CaCO3↓+2NaOH;
(3)碳酸钠溶液浓度大,不易产生浑浊;
[实验反思](1)探究碳酸钙能否溶解在碳酸钠溶液中;
(2)取2 mL饱和石灰水于试管中,滴加碳酸钠溶液.
点评 解答本题要掌握各种物质的性质方面的知识,只有这样才能对相关方面的问题做出正确的判断.

 阅读快车系列答案
阅读快车系列答案| A. |  氢气的验纯 | B. | 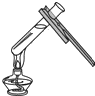 给盛有液体的试管加热 | ||
| C. | 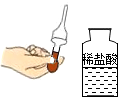 滴管取液后移动 | D. | 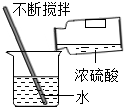 稀释浓硫酸 |
| A. | 水由水分子构成 | |
| B. | 水由氢原子和氧原子构成 | |
| C. | 水由氢、氧两种元素组成 | |
| D. | 一个水分子由两个氢原子和一个氧原子构成 |
| A. | NaCl、Na2CO3、KNO3 | B. | Ca(OH)2、KCl、K2CO3 | ||
| C. | H2SO4、Na2SO4、NaOH | D. | CuSO4、NaOH、Na2SO4 |
探究1:反应后所得溶液中溶质是什么?
【进行猜想】可能是MgCl2
【实验验证】
| 实验步骤 | 实验现象 | 实验结论 |
| 取反应后溶液少量于试管中,滴入NaOH溶液 | 产生白色沉淀 | 反应后所得溶液中溶质是MgCl2 |
| 另取反应后溶液少量于试管中,滴入硝酸银溶液和稀硝酸. |
【进行猜想】猜想一:可能是NH3;
猜想二:可能是氢气;
猜想三:可能是NH3和H2的混合气体;
【查阅资料】在百度网页中输入氨气的化学性质,可以获知氨气的部分化学性质如下:
①跟谁反应:NH3+H2O═NH3•H2O
②跟酸反应:NH3+HCl═NH4Cl 2NH3+H2SO4═(NH4)2SO4
③跟某些金属氧化物反应:3CuO+2NH3$\frac{\underline{\;△\;}}{\;}$3Cu+3H2O+N2
【实验探究】为了探究气体的成分,同学们设计了如下实验装置:
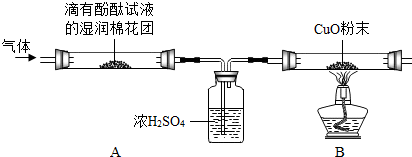
①A中观察到A中棉花团变红色,证明有NH3;
②B中玻璃管内观察到黑色粉末变红色,证明有H2;
③浓硫酸的作用是吸收氨气.
【实验结论】综合以上实验现象和分析,镁与NH4Cl反应的化学方程式为Mg+2NH4Cl=MgCl2+H2↑+2NH3↑.
| A. | 将农田中产生的秸秆就地焚烧 | B. | 将废旧电池深埋 | ||
| C. | 高炉炼铁的废气直接排放到大气中 | D. | 增加植树造林面积 |
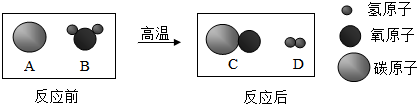
| A. | 该反应是置换反应 | B. | 图中气体单质的化学式为H2 | ||
| C. | 反应后原子的个数减少 | D. | 水煤气泄漏会污染空气 |
| A. | 在无色碘化钾溶液中滴加淀粉溶液,溶液变蓝 | |
| B. | 无色的氯化氢气体和氨气混合,产生白雾 | |
| C. | 在氢氧化钠稀溶液中滴加数滴硫酸铜溶液,产生蓝色絮状沉淀 | |
| D. | 无色碘化钾溶液中加入硝酸银溶液,产生白色沉淀 |