题目内容
11.下面对化学知识的归纳和整理,合理的是( )| A. | 电解水的生成物中有氢气和氧气,说明水中只含有氢元素和氧元素 | |
| B. | 生活中用加热煮沸的方法,可将硬水转化为软水 | |
| C. | 在密闭容器中点燃红磷,可以测定空气中氧气的质量分数 | |
| D. | 在盐酸中滴加氢氧化钠溶液,溶液的pH会增大 |
分析 A、根据电解水的生成物可得到水的组成;
B、生活中用加热煮沸的方法,能将硬水转化为软水;
C、在密闭容器中点燃红磷,可以测定空气中氧气的体积分数;
D、在盐酸中滴加氢氧化钠溶液,溶液的pH会增大.
解答 解:A、电解水的生成物中有氢气和氧气,说明水是由氢元素和氧元素组成的;错误;
B、硬水是含有较多钙、镁离子的水,加热煮沸时钙、镁离子会形成沉淀,水的硬度降低,因此加热煮沸能将硬水软化;说法正确.
C、在密闭容器中点燃红磷,可以测定空气中氧气的体积分数;说法错误
D、在盐酸中滴加氢氧化钠溶液,溶液的pH会增大.正确;
答案:BD.
点评 答本题要掌握溶液酸碱性和PH大小之间的关系,掌握物质的组成和反应类型的判断方法,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
相关题目
2.学校研究性学习小组选择探究“CuSO4溶液显蓝色与什么离子有关?”作为研究课题,以下是他们提交的实验方案,其中不需要做的实验是( )
| A. | 观察Na2SO4、K2SO4溶液的颜色 | |
| B. | 观察HNO3、Cu(NO3)2溶液的颜色 | |
| C. | 向CuSO4溶液中滴加适量的NaOH溶液,静置后观察溶液颜色 | |
| D. | 加水稀释后观察溶液的颜色 |
19.在化学实验室,某小组同学实验时发现一瓶没有密封好的NaOH已经结块.于是对其成分进行科学探究,请你一起完成探究的过程.
Ⅰ固体的成分分析
【提出问题】结块后的固体成分是什么?
【猜想与假设】
猜想一:固体为碳酸钠
猜想二:固体为碳酸钠和氢氧化钠.
用化学方程式表示固体中有碳酸钠的原因CO2+2NaOH═Na2CO3+H2O.
【查阅资料】BaCl2溶液pH=7
【实验探究】从瓶中取出一定量的固体,加入足量水溶解,再将溶液分三等份分别装入A、B、C三支试管,进行如图1所示实验.

甲同学根据实验现象,认为结块固体中有碳酸钠和氢氧化钠.
【实验分析】
(1)根据甲同学的实验结论可知,三支试管中观察到的实验现象分别为:A试管中溶液变红,B试管出现大量气泡,C试管中出现白色沉淀;C试管中现象产生的原因是(用化学方程式表示)Na2CO3+BaCl2=BaCO3↓+2NaCl.
(2)乙同学认为甲同学的结论是不正确的,原因是碳酸钠溶液呈碱性,也是无色酚酞变红.
【实验设计】请你设计合理的实验方案,填入下列表格中.
Ⅱ固体中各成分含量
为确定该固体样品中Na2CO3的质量分数,小芳同学称取2g样品,利用A为Y形管、B为量气管、C为水准管作为主要反应容器,进行了如图2(I)所示实验.
(1)在量气管内水面上架一薄层油,目的是防止二氧化碳溶于水;将Y形管(装置A)向左倾斜,硫酸流到样品中.
(2)使样品与稀硫酸反应的操作为将Y形管(装置A)向左倾斜,硫酸流到样品中.
(3)实验结束后,小芳同学读出量气管中的气体体积为22.4mL(已知该温度压强下,CO2的密度为1.965g/L),请你计算出样品中Na2CO3质量分数.(写出计算过程)
(4)小明同学设计如图2(Ⅱ)装置,分别测定反应前、反应后仪器以及仪器内物质的总质量,进行有关计算,实验操作中没有失误,多次测量的结果均偏大,你认为可能的原因是逸出的二氧化碳中含有水蒸汽.
Ⅰ固体的成分分析
【提出问题】结块后的固体成分是什么?
【猜想与假设】
猜想一:固体为碳酸钠
猜想二:固体为碳酸钠和氢氧化钠.
用化学方程式表示固体中有碳酸钠的原因CO2+2NaOH═Na2CO3+H2O.
【查阅资料】BaCl2溶液pH=7
【实验探究】从瓶中取出一定量的固体,加入足量水溶解,再将溶液分三等份分别装入A、B、C三支试管,进行如图1所示实验.

甲同学根据实验现象,认为结块固体中有碳酸钠和氢氧化钠.
【实验分析】
(1)根据甲同学的实验结论可知,三支试管中观察到的实验现象分别为:A试管中溶液变红,B试管出现大量气泡,C试管中出现白色沉淀;C试管中现象产生的原因是(用化学方程式表示)Na2CO3+BaCl2=BaCO3↓+2NaCl.
(2)乙同学认为甲同学的结论是不正确的,原因是碳酸钠溶液呈碱性,也是无色酚酞变红.
【实验设计】请你设计合理的实验方案,填入下列表格中.
| 操作 | 现象 | 结论 |
| 取少量结块固体于试管(或烧杯)中,加水使其完全溶解,加入过量的氯化钡或氯化钙溶液,静置后,向上层清液(或过滤后向滤液)中滴加几滴无色酚酞溶液 | 若溶液变红 | 固体为碳酸钠和氢氧化钠 |
为确定该固体样品中Na2CO3的质量分数,小芳同学称取2g样品,利用A为Y形管、B为量气管、C为水准管作为主要反应容器,进行了如图2(I)所示实验.
(1)在量气管内水面上架一薄层油,目的是防止二氧化碳溶于水;将Y形管(装置A)向左倾斜,硫酸流到样品中.
(2)使样品与稀硫酸反应的操作为将Y形管(装置A)向左倾斜,硫酸流到样品中.
(3)实验结束后,小芳同学读出量气管中的气体体积为22.4mL(已知该温度压强下,CO2的密度为1.965g/L),请你计算出样品中Na2CO3质量分数.(写出计算过程)
(4)小明同学设计如图2(Ⅱ)装置,分别测定反应前、反应后仪器以及仪器内物质的总质量,进行有关计算,实验操作中没有失误,多次测量的结果均偏大,你认为可能的原因是逸出的二氧化碳中含有水蒸汽.
6.化学实验时学生获得知识,形成能力的重要方法,下列实验操作方法合理的是( )
| A. | 干燥的药品可以直接放在托盘天平上称量质量 | |
| B. | 向容器中装药品时,应先装液体药品,再装固体药品 | |
| C. | 加热烧杯、试管中的液体时,需用酒精灯隔着石棉网加热 | |
| D. | 收集有氧气的集气瓶,应盖着毛玻璃片,正放在实验桌上 |
16.实验室中有久置的四瓶无色溶液,标签破损,只知道它们分别是稀硫酸、氢氧化钠溶液、碳酸钠溶液、氯化钠溶液.为鉴别它们,实验过程如下:
(1)甲同学取四中溶液少许于四支试管中,分别向其中滴加紫色石蕊试液,能鉴别出来的溶液是稀硫酸、氯化钠溶液.
(2)为鉴别剩余两种溶液,乙同学继续进行了以下实验设计.
(3)丙同学按照乙同学的方案进行实验,结果两支试管中都观察到了明显的现象,其可能的原因是氢氧化钠吸收空气中的二氧化碳生成了碳酸钠.
(4)实验结束后,同学们认为在实验室中使用和存放药品时应注意:①正确倾倒液体,保护好标签;②密封保存.
(1)甲同学取四中溶液少许于四支试管中,分别向其中滴加紫色石蕊试液,能鉴别出来的溶液是稀硫酸、氯化钠溶液.
(2)为鉴别剩余两种溶液,乙同学继续进行了以下实验设计.
| 实验操作 | 实验现象与化学方程式 |
| 分别取两溶液于两支试管中,分别向其中滴加稀盐酸. | 一支试管中有明显现象:有气体生成化学方程式:Na2CO3+2HCl═2NaCl+H2O+CO2↑. |
| 另一只试管中无明显现象 |
(4)实验结束后,同学们认为在实验室中使用和存放药品时应注意:①正确倾倒液体,保护好标签;②密封保存.
3.学会化学会帮助我们远离危险,下列做法安全的是( )
| A. | 进入矿井前做灯火实验 | |
| B. | 夜晚发现家用燃气泄漏需开灯检查 | |
| C. | 为了勤俭节约,可以食用霉变不严重的大米 | |
| D. | 浓硫酸滴在皮肤和衣物应先用大量水冲洗 |
20.决定元素化学性质的是( )
| A. | 质子数 | B. | 中子数 | C. | 电子总数 | D. | 最外层电子数 |
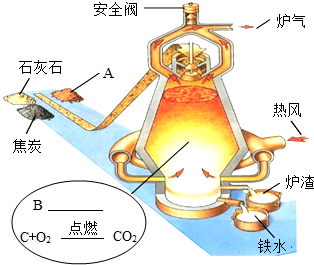 如图是炼铁高炉示意图,请写出物质A的名称铁矿石,B处的反应方程式为CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO,3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;该高炉中最终的产品为生铁.
如图是炼铁高炉示意图,请写出物质A的名称铁矿石,B处的反应方程式为CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO,3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;该高炉中最终的产品为生铁.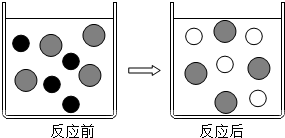 组成相似的盐具有一些相似的化学性质.
组成相似的盐具有一些相似的化学性质. ”代表的是硫酸根离子(填名称).
”代表的是硫酸根离子(填名称).