题目内容
13.如图是实验室常用的实验仪器与装置,根据所学知识回答下列问题:
(1)写出图中编号仪器名称:①酒精灯,②集气瓶.
(2)用高锰酸钾制取氧气时,所选用的发生装置是A(填装置序号),该装置还需添加的实验用品为棉花,反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,若用D装置用排水法来收集氧气,则导管a应接e导管口.
(3)用装置B制二氧化碳,其反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,但该同学发现试管内持续有气泡产生,但集气瓶中一直收集不满,怀疑装置漏气,请你帮他想个简单办法找出漏气部位在可能漏气的部位用肥皂水(水)涂抹,看是否有气泡.若用过氧化氢溶液和二氧化锰粉末制取氧气,不能(填“能”或“不能”)用B装置控制反应的发生与停止.
(4)某同学用E装置进行过滤,才过滤一会儿就发现过滤速度越来越慢,他应该采取的措施为①③(填序号).
①将要过滤的液体加明矾静置后再过滤 ②用玻璃棒在漏斗内搅拌以加快过滤速度
③重新更换滤纸继续过滤 ④将滤纸捣破可以加快过滤速度.
分析 (1)熟记常见仪器的名称;
(2)高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气; 结合注意事项来分析;
(3)根据制取二氧化碳的原理、检查装置气密性的方法以及装置的特点来分析;
(4)如果滤纸没有紧贴漏斗内壁,将会导致过滤速度过慢.
解答 解:(1)①是酒精灯,②是集气瓶;故填:酒精灯;集气瓶;
(2)高锰酸钾受热分解的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;属于固体加热制取气体,选择装置A;为了防止高锰酸钾进入集气瓶,应该在试管口塞一团棉花.氧气的密度比水小,所以氧气从短管进入.故填:A;棉花;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$ K2MnO4+MnO2+O2↑;e;
(3)实验室中,常用碳酸钙与稀盐酸反应来制取二氧化碳;在可能漏气的部位用肥皂水(水)涂抹,看是否有气泡;B装置可以控制反应的发生与停止,但隔板上放置的应该是块状固体而不能是粉末状固体,故实验室用过氧化氢溶液和二氧化锰粉末制取氧气不能用该装置;
故填:CaCO3+2HCl=CaCl2+H2O+CO2↑;在可能漏气的部位用肥皂水(水)涂抹,看是否有气泡;不能;
(4)如果难溶性固体过多会堵塞滤纸造成速度较慢;滤纸没有紧贴漏斗内壁,将会导致过滤速度过慢;可将要过滤的液体加明矾静置后再过滤或重新更换滤纸继续过滤;不可用玻璃棒进行搅拌,以免损坏滤纸,也不可将滤纸捣破,那就失去了过滤的意义.故填:①③.
点评 本题考查了实验室制气体的依据、反应原理以及气体的干燥,综合性比较强,要充分利用题目给出的信息进行理解运用.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
3.一种新型的甜味剂木糖醇在市场上大受欢迎.木糖醇的化学式为C5H12O5,它最大的优势是可以减少或者预防蛀牙.木糖醇的甜度与蔗糖相当,但热量只有蔗糖的60%.据介绍,木糖醇是一种原产于芬兰的天然甜味剂,后来日本从白桦树和玉米芯等植物中提炼出这种天然甜味剂.由于木糖醇不能被细菌分解,利用它来取代甜品中的糖分,可以防止蛀牙.而在口香糖里添加木糖醇是目前国际上最为普遍的防蛀方法.
(1)木糖醇是一种有机化合物(填“有机化合物”或“无机化合物”),属于营养素中的糖类,相对分子质量为152.
(2)请你设计实验证明木糖醇中含有碳元素和氢元素.
(1)木糖醇是一种有机化合物(填“有机化合物”或“无机化合物”),属于营养素中的糖类,相对分子质量为152.
(2)请你设计实验证明木糖醇中含有碳元素和氢元素.
| 操作 | 现象 | 结论 |
1.把木糖醇灼烧,再罩上一干冷的烧杯 2.迅速倒立烧杯,滴加澄清石灰水 | 烧杯内壁有水珠 石灰水变浑浊 | 木糖醇中含有氢元素 木糖醇中含有碳元素 |
8.我国科学家屠呦呦因为发现青蒿素,获得2015年诺贝尔医学奖.青蒿素是治疗疟疾的特效药,化学式可表示为C15H22O5,下列关于青蒿素的说法正确的是( )
| A. | 青蒿素含有42个原子 | B. | 青蒿素属于氧化物 | ||
| C. | 青蒿素中C、H、O的质量比是15:22:5 | D. | 青蒿素中碳元素质量分数最高 |
18.锆(Zr)的一种氧化物是耐高温的新型陶瓷材料.经测定锆的相对原子质量为91,其氯化物的相对分子质量为233.若锆在氯化物和这种氧化物中的化合价相同,则该氧化物的化学式为( )
| A. | Zr2O | B. | ZrO | C. | Zr2O3 | D. | ZrO2 |
2.蛋白质可以维持人体的生长发育和组织更新,下列食物中富含蛋白质的是( )
| A. | 馒头 | B. | 豆制品 | C. | 植物油 | D. | 水 |
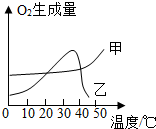 实验室常用二氧化锰催化分解过氧化氢的方法制取氧气,请写出反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.某同学从课外读物中得知新鲜的动物肝脏中有较多的过氧化氢酶,过氧化氢酶与无机催化剂Fe3+都可以催化过氧化氢分解.
实验室常用二氧化锰催化分解过氧化氢的方法制取氧气,请写出反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.某同学从课外读物中得知新鲜的动物肝脏中有较多的过氧化氢酶,过氧化氢酶与无机催化剂Fe3+都可以催化过氧化氢分解.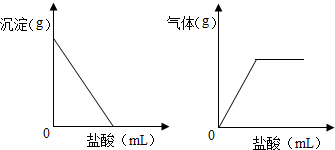 有一包白色固体,可能含有硫酸钠、碳酸钠、氯化钡、氢氧化钠中的一种或几种,取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加盐酸,沉淀的量、产生气体的量与加入盐酸体积的关系如图所示,由此推断白色固体中一定存在Na2CO3、BaCl2,一定不存在Na2SO4(均填写化学式).
有一包白色固体,可能含有硫酸钠、碳酸钠、氯化钡、氢氧化钠中的一种或几种,取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加盐酸,沉淀的量、产生气体的量与加入盐酸体积的关系如图所示,由此推断白色固体中一定存在Na2CO3、BaCl2,一定不存在Na2SO4(均填写化学式).