题目内容
10.维生素A有维生素A1(C20H3lO)和维生素A2 (C20H28O).下列说法不正确的是( )| A. | 维生素A可以预防夜盲症 | |
| B. | 1个维生素A1分子比1个维生素A2分子多2个原子 | |
| C. | 维生素A1和维生素A2组成元素相同,化学性质也相同 | |
| D. | 维生素A1中氧元素比维生素A2中元素质量分数低 |
分析 A.根据维生素A的生理功能来分析;
B.根据分子结构来分析解答;
C.根据物质的组成与结构来分析;
D.根据化合物中元素的质量分数的比较方法来分析.
解答 解:A.维生素A可以预防夜盲症,故正确;
B.由化学式可知,1个维生素A1分子中含有52个原子,1个维生素A2分子中含有49个原子,可见1个维生素A1分子比1个维生素A2分子多2个原子,故正确;
C.维生素A1和维生素A2组成元素相同,但是分子结构不同,所以化学性质性质不同,故错误;
D.维生素A1(C20H3lO)中氧元素的质量分数为:$\frac{16}{12×20+1×31+16}×100%$;维生素A2中氧元素的质量分数为:$\frac{16}{12×20+1×28+16}×100%$,可见维生素A1中氧元素比维生素A2中氧元素质量分数低,故正确.
故选C.
点评 本题难度不大,考查同学们灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
20.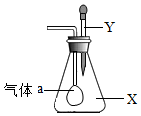 如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起.气体X和液体Y可能是( )
如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起.气体X和液体Y可能是( )
 如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起.气体X和液体Y可能是( )
如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起.气体X和液体Y可能是( )| A. | X是CO2,Y是氢氧化钠 | B. | X是O2,Y是稀H2SO4(稀硫酸) | ||
| C. | X是N2,Y是稀盐酸 | D. | X是CO,Y是氢氧化钠 |
1.稀土金属是我国战略性资源,应加以保护.稀土金属钇(Y)是很活泼的金属常见化合价为+3价.它是激光和超导的重要材料.我国蕴藏着丰富的钇矿石(Y2FeBe2Si2O10),以此矿石为原料生产氧化钇(Y2O3)的主要流程如下: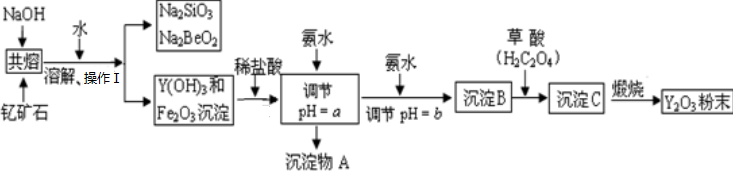
资料卡:①有关金属离子形成氢氧化物沉淀时的pH如下表:
②铁离子遇到KSCN溶液会呈现血红色
(1)已知钇矿石中Be为+2价,Si为+4价,则Fe的化合价为+2;
(2)操作Ⅰ是过滤;
(3)加盐酸时,发生的中和反应的方程式为:Y(OH)3+3HCl═YCl3+3H2O;
(4)调节pH=a,则a应控制在3.7~6.0的范围内,检验Fe3+是否沉淀完全的操作方法是取溶液适量于试管中,滴加KSCN溶液,如果溶液呈现血红色,说明铁离子没有完全沉淀,如果溶液呈现无色,说明铁离子完全沉淀.

资料卡:①有关金属离子形成氢氧化物沉淀时的pH如下表:
| 开始沉淀时的pH | 完全沉淀时的pH | |
| Fe3+ | 2.7 | 3.7 |
| Y3+ | 6.0 | 8.2 |
(1)已知钇矿石中Be为+2价,Si为+4价,则Fe的化合价为+2;
(2)操作Ⅰ是过滤;
(3)加盐酸时,发生的中和反应的方程式为:Y(OH)3+3HCl═YCl3+3H2O;
(4)调节pH=a,则a应控制在3.7~6.0的范围内,检验Fe3+是否沉淀完全的操作方法是取溶液适量于试管中,滴加KSCN溶液,如果溶液呈现血红色,说明铁离子没有完全沉淀,如果溶液呈现无色,说明铁离子完全沉淀.
18.下列图象能正确反映对应的变化关系的是( )
| A. |  利用红磷燃烧测定空气中氧气的含量(打开止水夹前) | |
| B. |  将生锈严重的铁钉加入到足量的稀盐酸中 | |
| C. | 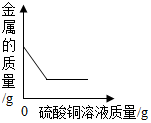 向一定量铁粉和铜粉混合物中加入硫酸铜溶液 | |
| D. |  将过量的等质量的镁和锌跟别加入到等质量、等质量分数的稀盐酸中 |
15.某金属加工厂生产过程中的废液含有少量硝酸银和硝酸铜,为回收利用资源和防止污染,向废液中加入一定量的铁粉,反应停止后过滤,向滤出的固体中加入少量稀盐酸,无气体产生.则下列有关说法中,不正确的是( )
| A. | 滤出的固体中一定含有银,一定不含铁 | |
| B. | 滤出的固体中一定含有银,可能含有铜 | |
| C. | 滤液中一定有硝酸银,可能有硝酸铜 | |
| D. | 滤液中若有硝酸银,则一定有硝酸铜 |
19.下列物质,属于纯净物的是( )
| A. | 空气 | B. | 矿泉水 | C. | 苹果汁 | D. | 蒸馏水 |
20.下列图示的实验操作不正确的是( )
| A. |  过滤 | B. |  检查气密性 检查气密性 | C. |  测溶液pH值 测溶液pH值 | D. |  用滴管取用液体 |
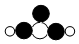
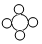
 分别表示H、C、N、O四种原子,下列各项中表示有机物的是( )
分别表示H、C、N、O四种原子,下列各项中表示有机物的是( )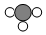

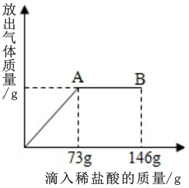 在一烧杯中盛有由Na2CO3和NaCl 组成的固体混合物25g,向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的质量与滴入稀盐酸的质量关系如图所示(已知反应的化学方程式为:Na2CO3+2HCl=2NaCl+CO2↑+H2O).请分析曲线图后回答下列问题:
在一烧杯中盛有由Na2CO3和NaCl 组成的固体混合物25g,向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的质量与滴入稀盐酸的质量关系如图所示(已知反应的化学方程式为:Na2CO3+2HCl=2NaCl+CO2↑+H2O).请分析曲线图后回答下列问题: