题目内容
加热KClO3与MnO2混合物,使KClO3完全分解。在t℃时将残留物加入10g水中,充分搅拌后有7.6g固体未溶;保持温度不变,再加入5g水,仍有5g固体未溶,t℃时KCl的溶解度不可能是( )A.15.2g B.52g C.65.2g D.91.2g
答案:A
解析:
提示:
解析:
| 精析 饱和溶液指的是在一定温度下、在一定量溶剂中不能再溶解某溶质的溶液,饱和溶液是溶解度计算的基础,也是溶质质量分数计算中一个值得注意的信号。由于题意交待清楚,故第二次加水时未溶的5g固体的组成有两种可能的情况:
(1)是KCl和MnO2的混合物,在这种情况下t℃时5g水溶解KCl为(7.6-5)g=2.6g恰好饱和,所以t℃时KCl的溶解度为 (2)只看MnO2,这种情况下7.6g固体中KCl的质量为(7.6-5)g=2.6g,这又有两种可能情况: 一是溶解这2.6gKCl恰好需5g水t℃下KCl的溶解度仍为52g; 二是溶解这2.6gKCl所需水的质量小于5g,t℃下KCl的溶解度应大于52g。 由上可见,不论哪种情况,t℃时KCl的溶解度都不会小于52g,即应选A。
|
提示:

练习册系列答案
相关题目
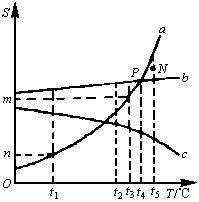

 如图是实验室加热KClO3与MnO2的混合物制取氧气的装置图.
如图是实验室加热KClO3与MnO2的混合物制取氧气的装置图.