题目内容
12.如图是初中化学中常见物质间的转化关系(部分反应物、生成物未列出,每步反应均完全),其中A是一种建筑材料的主要成分,B是一种黑色粉末,C是气体,E为蓝色溶液,X的俗名叫苏打.试回答下列有关问题::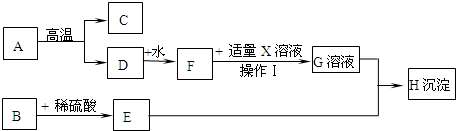
(1)写出有关物质的化学式:A:CaCO3;C:CO2;X:Na2CO3
(2)由F与X反应后得到G溶液的实验操作Ⅰ名称是过滤
(3)写出G+E→H的化学方程式:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
(4)上图中,按单质、氧化物、酸、碱、盐进行分类,一定没有的物质类别是单质.
分析 根据A是一种建筑材料的主要成分,A高温会生成C和D,所以A就是碳酸钙,碳酸钙高温会分解成氧化钙和二氧化碳,C是气体,所以C是二氧化碳,D就是氧化钙,水喝氧化钙反应生成氢氧化钙,所以F就是氢氧化钙,X的俗名叫苏打,所以X是碳酸钠,黑色的粉末和硫酸反应会生成蓝色的溶液E,所以B是氧化铜,E是硫酸铜,氢氧化钙和碳酸钠反应会生成碳酸钙沉淀和氢氧化钠,所以G是氢氧化钠,氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,所以H是氢氧化铜沉淀,然后将推出的物质进行验证即可.
解答 解:(1)A是一种建筑材料的主要成分,A高温会生成C和D,所以A就是碳酸钙,碳酸钙高温会分解成氧化钙和二氧化碳,C是气体,所以C是二氧化碳,D就是氧化钙,水喝氧化钙反应生成氢氧化钙,所以F就是氢氧化钙,X的俗名叫苏打,所以X是碳酸钠,黑色的粉末和硫酸反应会生成蓝色的溶液E,所以B是氧化铜,E是硫酸铜,氢氧化钙和碳酸钠反应会生成碳酸钙沉淀和氢氧化钠,所以G是氢氧化钠,氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,所以H是氢氧化铜沉淀,经过验证,推导正确,所以A是CaCO3,C是CO2,X是Na2CO3;(2)过滤是将固体和液体进行分离的一种操作,F和X反应后生成碳酸钙沉淀和氢氧化钠,所以由F与X反应后得到G溶液的实验操作应是过滤;(3)G+E→H的反应是氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,化学方程式为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;(4)二氧化碳是氧化物,硫酸是酸,氢氧化钠是碱,碳酸钙碳酸钠是盐,没有单质.给答案为:(1)CaCO3,CO2,Na2CO3;(2)过滤;(3)CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;(4)单质.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

| A. |  | B. |  | C. |  | D. |  |
| A. | 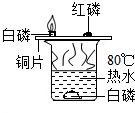 探究燃烧条件 | B. | 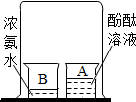 探究分子运动 | ||
| C. | 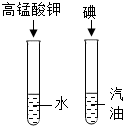 探究影响溶解度的因素 | D. | 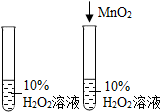 探究二氧化锰对反应速率的影响 |
| A. | 水是由氢元素和氧元素组成的氧化物 | |
| B. | 用肥皂水可区分硬水和软水 | |
| C. | 电解水的微观过程中不能说明化学反应中分子可以再分 | |
| D. | 净化水的常用方法有吸附、沉淀、过滤和蒸馏 |
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 (g/100g水) | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
(2)60℃时在100g水中加入100g硝酸钾固体,充分溶解后所形成的溶液是不饱和溶液(“饱和”或“不饱和”).
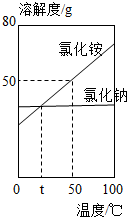 NH4Cl和NaCl的溶解度随温度变化如图所示,下列说法正确的是( )
NH4Cl和NaCl的溶解度随温度变化如图所示,下列说法正确的是( )| A. | NH4Cl的溶解度一定大于NaCl | |
| B. | 将NaCl溶液降温一定会有NaCl固体析出 | |
| C. | 50℃时饱和溶液的溶质质量分数为50% | |
| D. | 将t℃时,NH4Cl和NaCl的饱和溶液加热至50℃,两溶液的溶质质量分数相等 |
 A-H是初中化学中的常见物质,AB都是黑色固体,D是紫红色固体,AD都是单质,G的俗名叫熟石灰,F的俗名叫苏打,H是含有二种元素的一种常见酸,物质之间的关系如图.(“--”表示两种物质会发生反应,“→”表示前者通过反应能生成后者)
A-H是初中化学中的常见物质,AB都是黑色固体,D是紫红色固体,AD都是单质,G的俗名叫熟石灰,F的俗名叫苏打,H是含有二种元素的一种常见酸,物质之间的关系如图.(“--”表示两种物质会发生反应,“→”表示前者通过反应能生成后者)