题目内容
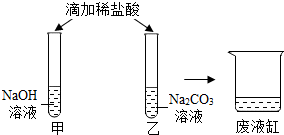
某厂废液中的溶质只含有少量硫酸和硫酸钠,取废液样品30 g于小烧杯中(经测定该废液样品中含水的质量是29.22g),向其中慢慢滴加2%的NaOH溶液20g,并不断搅拌,恰好完全反应,所得溶液为不饱和溶液。(提示: H2SO4+2NaOH=Na2SO4+2H2O)
(1)计算该废液中硫酸的质量。
(2)恰好反应时,所得溶液溶质的质量分数。
(1) 解:设30g废液中硫酸的质量为x,反应生成硫酸钠的质量为y
H2SO4 +2NaOH =Na2SO4 + 2H2O
98 80 142
 x 20 g×2% y
x 20 g×2% y
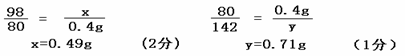
(2)30g 废液中含硫酸钠的质量:30g-29.22g-0.49g=0.29g (1分)
恰好反应时,所得硫酸钠溶液的溶质质量分数为:
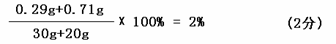
答:废液中硫酸的质量为0.49g,恰好反应时,所得硫酸钠溶液的溶质质量分数为2% 。
(评分标准:设、答、单位及格式错误共计扣除0.5分,不累加;其它合理解法可参照给分。如果解法思路正确,计算部分出现错误可酌情给分)

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目