题目内容
4.某兴趣小组为探究活泼金属与酸反应的规律,将质量相等、颗粒大小相同的甲、乙两种金属分别放入到质量分数相同的足量稀硫酸中,出生成氢气的质量与反应时间的关系如图A所示.则乙种金属的活动性顺序强.若同时将甲、乙两种金属分别放入到图B装置中,直到反应结束,结合图A的信息描述天平指针的指向变化天平指针先偏左后偏右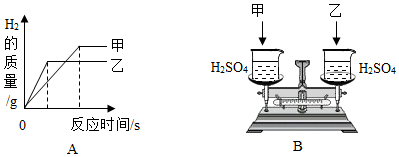
分析 根据金属活动性强的金属与酸反应时,速率快;依据图象可以看出甲生成的氢气多进行分析.
解答 解:金属活动性强的金属与酸反应时,速率快,乙金属先出现转折点,所以乙种金属的活动性顺序强;依据图象可以看出甲生成的氢气多,乙金属活泼,所以刚开始,反应速率快,生成氢气多,但是反应最后,甲生成的氢气多,所以天平指针的指向变化是:天平指针先偏左后偏右.
故答案为:乙,天平指针先偏左后偏右.
点评 对于活泼金属,活动性越强的金属与酸反应越剧烈,即反应放出氢气的速度越快.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
19.以下是我们温州的部分文化遗产,其制作过程主要属于化学变化的是( )
| A. | 温州剪纸 | B. | 平阳木偶雕刻 | C. | 泰顺米酒 | D. | 乐清黄杨木雕 |
9.下列化学反应中既不属于化合反应也不属于分解反应的是( )
| A. | CaO+H2O=Ca(OH)2 | B. | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ | ||
| C. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | D. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O |

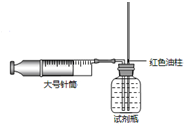 小李学习了二氧化碳知识后,进行了二氧化碳气体在水中溶解性的探究,其实验步骤及装置如下.
小李学习了二氧化碳知识后,进行了二氧化碳气体在水中溶解性的探究,其实验步骤及装置如下.