题目内容
5.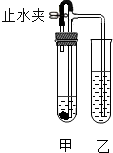 某同学用如图所示装置进行实验(图中铁架台等仪器均已略去).在甲试管中加入试剂后,塞紧橡皮塞,立即打开止水夹,乙试管中有气泡冒出;一段时间后关闭止水夹,乙试管中液面上升,溶液由澄清变浑浊.符合上述实验现象的甲、乙试管中应加入的试剂是( )
某同学用如图所示装置进行实验(图中铁架台等仪器均已略去).在甲试管中加入试剂后,塞紧橡皮塞,立即打开止水夹,乙试管中有气泡冒出;一段时间后关闭止水夹,乙试管中液面上升,溶液由澄清变浑浊.符合上述实验现象的甲、乙试管中应加入的试剂是( )| A | B | C | D | |
| 甲 | Zn、稀H2SO4 | Cu、稀H2SO4 | CaCO3、稀HCl | Na2CO3、稀H2SO4 |
| 乙 | BaCl2 | Ba(OH)2 | KNO3 | NaCl |
| A. | A | B. | B | C. | C | D. | D |
分析 本题主要考查物质之间反应的现象,利用该装置的特征,打开止水夹时,I中两种物质反应会生成气体,气体通过导气管进入Ⅱ中,Ⅱ中才会看到气泡;关闭止水夹时,I中生成的气体排不出去,气压增大,会把I中的液体压入Ⅱ中,与Ⅱ中的液体反应会生成沉淀,溶液由无色变为浑浊.根据以上分析,结合四个选项中物质间反应的现象进行解答.
解答 解:
A、I中锌和稀硫酸反应会生成氢气,打开止水夹时,Ⅱ中会看到气泡,关闭止水夹后,I中氢气不断生成,压强增大,将I中液体压入Ⅱ中,稀硫酸和硫酸锌会与氯化钡溶液会反应生成硫酸钡白色沉淀,溶液由无色变为浑浊,符合实验现象,所以A正确;
B、I中铜和稀硫酸不反应,Ⅱ中不会看到气泡,关闭止水夹后也不会有液体被压入Ⅱ中,溶液也不会变浑浊,不符合实验现象,故B不正确;
C、I中碳酸钙和盐酸反应会生成气体二氧化碳,打开止水夹时,Ⅱ中会看到气泡,但是二氧化碳和硝酸钾不反应,不会出现沉淀,被压入的稀盐酸和氯化钙与硝酸钾也不反应,看不到溶液变浑浊变,不符合实验现象,故C错误;
D、I中碳酸钠和稀硫酸反应会生成气体二氧化碳,打开止水夹时,Ⅱ中会看到气泡,但是二氧化碳和氯化钠不反应,关闭止水夹后,被压入的稀硫酸和氯化钠也不反应,硫酸钠与氯化钠不反应,看不到浑浊,不符合实验现象,故D错误.
故选A.
点评 本题考查物质间的反应现象,我们要能根据该装置的特点及物质间的反应分析实验现象.

练习册系列答案
相关题目
15.椰树牌矿泉水的成分有:钠31mg/L,钙35.11mg/L,碘0.051mg/L等,这里所标的各成分指的是( )
| A. | 单质 | B. | 元素 | C. | 原子 | D. | 分子 |
16.小强同学前往当地的石灰石矿区进行调查,他取回了若干块矿石样品,对样品中的碳酸钙的质量分数进行测验采取了以下方法,取用8g这种石灰石样品,把40g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的杂质不溶于水,也不与盐酸反应).请回答下列问题:
(1)发生反应的化学方程式为CaCO3+2HC1═CaC12+H2O+CO2↑
(2)M的值为3
(3)石灰石样品中碳酸钙的质量分数85%
(4)以上实验中产生的二氧化碳的总量(x)的比例式为$\frac{100}{6.8g}=\frac{44}{x}$
(5)将第二次实验后得到的混合物过滤,要将得到的滤液变成溶质质量分数为10%的溶液,应向溶液中加水32.7g
(6)用36.5%的浓盐酸配制实验中使用的40g稀盐酸,需要加水的质量是20g.
| 序号 | 加入稀盐酸的质量(g) | 剩余固体的质量(g) |
| 第1次 | 10 | 5.5 |
| 第2次 | 10 | M |
| 第3次 | 10 | 1.2 |
| 第4次 | 10 | 1.2 |
(2)M的值为3
(3)石灰石样品中碳酸钙的质量分数85%
(4)以上实验中产生的二氧化碳的总量(x)的比例式为$\frac{100}{6.8g}=\frac{44}{x}$
(5)将第二次实验后得到的混合物过滤,要将得到的滤液变成溶质质量分数为10%的溶液,应向溶液中加水32.7g
(6)用36.5%的浓盐酸配制实验中使用的40g稀盐酸,需要加水的质量是20g.
20.下列依据实验目的进行的实验设计,合理的是( )
| 选项 | 实验目的 | 实验设计 |
| A | 从空气中获取纯净的氮气 | 用硫燃烧除去空气中的氧气 |
| B | 鉴别硬水和软水 | 观察颜色或闻气味 |
| C | 除去混在二氧化碳中的氯化氢气体 | 把混合气体通过足量的氢氧化钠溶液 |
| D | 鉴别硝酸铵和氯化钠固体 | 加适量的水溶解,测量前后温度变化 |
14.下列物质的用途主要是利用其化学性质的是( )
| A. | 铜作电线 | B. | 天燃气作燃料 | ||
| C. | 不锈钢制炊具 | D. | 氢气填充探空气球 |
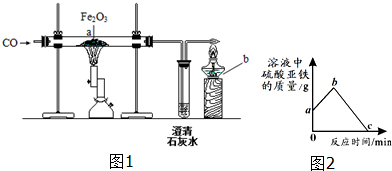
 某学校科学兴趣小组为了探究实验室中久置的NaOH的变质程度,具体如图:
某学校科学兴趣小组为了探究实验室中久置的NaOH的变质程度,具体如图: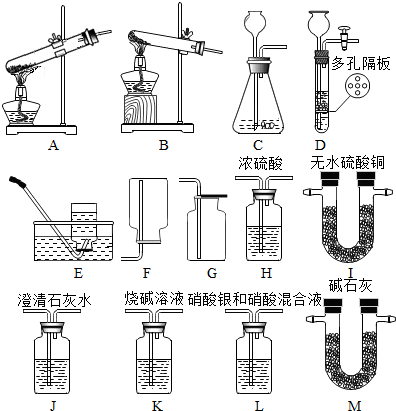
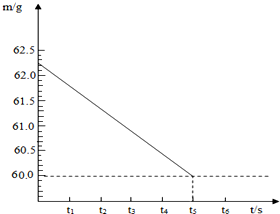 小红发现松软的面包、酥脆的饼干内部都有许多小孔(如图所示).为探究这个问题,她从面点师那里了解到:此类食品制作过程中加入膨松剂,碳酸氢钠就是一种常用的膨松剂.小红从超市买来一袋膨松剂(碳酸氢钠),按照研究物质的一般方法,对其进行探究.
小红发现松软的面包、酥脆的饼干内部都有许多小孔(如图所示).为探究这个问题,她从面点师那里了解到:此类食品制作过程中加入膨松剂,碳酸氢钠就是一种常用的膨松剂.小红从超市买来一袋膨松剂(碳酸氢钠),按照研究物质的一般方法,对其进行探究.