题目内容
10.乙炔(C2H2)气体和氧气反应能产生高温火焰,工业生产中常用氧炔焰切割或焊接金属.乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时生成一种白色固体.【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下几种可能:
猜想一:Ca(OH)2;猜想二:CaCO3;猜想三:CaO他的依据是质量守恒定律
【交流反思】经过同学们交流讨论,认为猜想三不成立.否定猜想三的理由是:氧化钙易与水反应生成氢氧化钙
【进行实验】
(1)取少量白色固体放入试管中,滴加稀盐酸,没有观察到气泡出现,证明猜想二不成立.
(2)取少量白色固体加入到水中,取上层清液,加入碳酸钠溶液,有白色沉淀出现,证明猜想一成立.该反应的化学方程式为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
结论:白色固体是Ca(OH)2.
【拓展】已知碳化钙与水反应非常剧烈,并生成易燃易爆的乙炔气体.实验室应将碳化钙密封保存,并远离热源.碳化钙与水反应的化学方程式是CaC2+2H2O=C2H2↑+Ca(OH)2.
分析 【做出猜想】
白色固体可能是Ca(OH)2;也可能是CaCO3;也可能是CaO;
【交流反思】
氧化钙能和水反应生成氢氧化钙;
【进行实验】
氢氧化钙和稀盐酸反应生成氯化钙和水,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;
氢氧化钙能和碳酸钠反应生成白色沉淀碳酸钙和氢氧化钠;
根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式.
解答 解:【做出猜想】
猜想一:Ca(OH)2;猜想二:CaCO3;猜想三:CaO;他的依据是质量守恒定律,因为反应前后元素的种类不变,原子的种类和个数都不变.
故填:CaCO3;质量守恒定律.
【交流反思】
猜想三不成立的理由是氧化钙易与水反应生成氢氧化钙.
故填:氧化钙易与水反应生成氢氧化钙.
【进行实验】
(1)取少量白色固体放入试管中,滴加稀盐酸,没有观察到气泡出现,证明猜想二不成立;
(2)取少量白色固体加入到水中,取上层清液,加入碳酸钠溶液,有白色沉淀出现,证明猜想一成立,该反应的化学方程式为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
故填:气泡出现;加入碳酸钠溶液;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
【拓展】
碳化钙与水反应非常剧烈,并生成易燃易爆的乙炔气体.实验室应将碳化钙密封保存,并远离热源;
碳化钙与水反应的化学方程式为:CaC2+2H2O=C2H2↑+Ca(OH)2.
故填:密封;CaC2+2H2O=C2H2↑+Ca(OH)2.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
1.氧原子的半径和质量大小的数量级是( )
| A. | 10-10米;10-27千克 | B. | 10-8米;10-26千克 | ||
| C. | 10-10米;10-26千克 | D. | 10-8米;10-27千克 |
17.下列化学方程式书写正确的是( )
| A. | Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO | B. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | ||
| C. | CO2+Ca(OH)2═CaCO3+H2O | D. | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ |

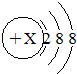 如图所用粒子结构示意图表示粒子按要求填空:
如图所用粒子结构示意图表示粒子按要求填空: