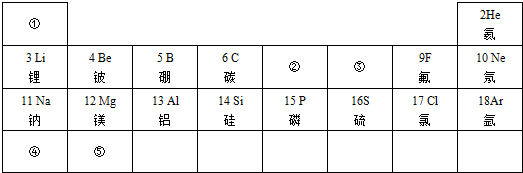
题目内容
2.生产、生活中处处有化学.(1)自来水厂净水过程中用到活性炭,这是利用了活性炭的吸附性.
(2)合金的用途广泛,下列物质不属于合金的是③性.(选填序号).
①黄铜②不锈钢③铁矿石
(3)自行车链条常采用涂油的方法防锈.
(4)高铁酸钠(Na2FeO4)是一种新型高效净水剂,高铁酸钠中铁元素的化合价是+6.
(5)用碳酸氢钠治疗胃酸过多的反应原理是:NaHCO3+HCl=NaCl+H2O+CO2↑ (用化学方程式表示)
分析 (1)根据活性炭的吸附性分析.
(2)根据合金的特征分析判断;
(3)自行车链条常采用涂油的方法防锈.
(4)根据化合价原则求出元素的化合价.
(5)根据碳酸氢钠与盐酸的反应分析回答.
解答 解:(1)自来水厂净水过程中用到活性炭,这是利用了活性炭的吸附性.
(2)合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的物质,黄铜、不锈钢属于合金,铁矿石不属于合金.
(3)自行车链条常采用涂油的方法防锈.
(4)在高铁酸钠(Na2FeO4)中,钠元素显+1价,氧元素显-2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-2)×4=0,则x=+6价.
(5)用碳酸氢钠治疗胃酸过多,是碳酸氢钠与盐酸发生了反应,方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑.
故答为:(1)吸附; (2)③;(3)涂油; (4)+6;(5)NaHCO3+HCl=NaCl+H2O+CO2↑.
点评 生产、生活中处处有化学,学会利用化学的知识来分析解答问题的方法是解答本题的关键.

练习册系列答案
 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
12.如图所示的四个图象,不能正确反映对应变化关系的是( )
| A. | 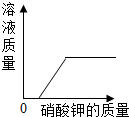 一定温度下,向一定量接近饱和的硝酸钾溶液中加入硝酸钾 | |
| B. | 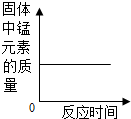 加热一定量的高锰酸钾固体 | |
| C. | 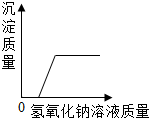 向一定量硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液 | |
| D. | 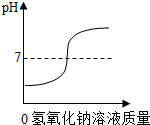 向稀盐酸中逐滴加入过量的氢氧化钠溶液 |
17.如图所示的四个图象,不能正确反映对应变化关系的是( )
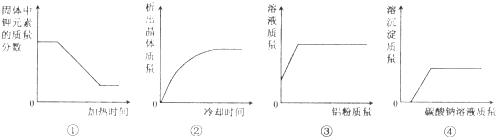

| A. | ①加热一定质量的氯酸钾与二氧化锰混合物 | |
| B. | ②将某温度下热的硝酸钾饱和溶液逐渐冷却至室温 | |
| C. | ③向一定量硫酸铜溶液中加入铝粉 | |
| D. | ④向一定量的实验室制取二氧化碳后残留的酸性废水中加入过量碳酸钠溶液 |
7.物质的性质与构成物质的微粒和结构有密切的关系.下列有关说法不正确的是( )
| A. | 金刚石和石墨的物理性质不同,是由于构成它们的碳原子结构不同 | |
| B. | 一氧化碳和二氧化碳的化学性质不同,是由于构成它们的分子不同 | |
| C. | 生铁和钢的性能不同,主要是由于它们的含碳量不同 | |
| D. | 稀盐酸和稀硫酸具有不同的化学性质,是由于它们的阴离子不同 |
2.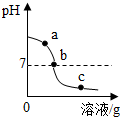 为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,小鸣和同学们通过测定了反应后溶液的pH,得到了如图所示的pH曲线,请回答:
为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,小鸣和同学们通过测定了反应后溶液的pH,得到了如图所示的pH曲线,请回答:
(1)由图可知该实验操作是将稀盐酸滴加到另一种溶液中;
(2)该反应的化学方程式为Ca(OH)2+2HCl═CaCl2+2H2O;
(3)实验过程中,小鸣取了a、b、c三处反应后的溶液于三
个烧杯中,却忘了作标记,请你设计不同的方案(不再
用测定pH的方法),探究三种样品分别属于哪处溶液.
【查阅资料】CaCl2溶液显中性,CaCl2+Na2CO3=CaCO3↓+2NaCl.
【探究过程】
①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现溶液由无色变成红色 的现象.结论:该样品是a处溶液.
②为进一步确定b或c处溶液,又设计了以下方案:
 为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,小鸣和同学们通过测定了反应后溶液的pH,得到了如图所示的pH曲线,请回答:
为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,小鸣和同学们通过测定了反应后溶液的pH,得到了如图所示的pH曲线,请回答:(1)由图可知该实验操作是将稀盐酸滴加到另一种溶液中;
(2)该反应的化学方程式为Ca(OH)2+2HCl═CaCl2+2H2O;
(3)实验过程中,小鸣取了a、b、c三处反应后的溶液于三
个烧杯中,却忘了作标记,请你设计不同的方案(不再
用测定pH的方法),探究三种样品分别属于哪处溶液.
【查阅资料】CaCl2溶液显中性,CaCl2+Na2CO3=CaCO3↓+2NaCl.
【探究过程】
①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现溶液由无色变成红色 的现象.结论:该样品是a处溶液.
②为进一步确定b或c处溶液,又设计了以下方案:
| 实验步骤 | 实验现象 | 实验结论 |
| 另取余下的少量样品分别放于两支试管中,并分别滴加足量的Na2CO3溶液. | 只产生白色沉淀 | 该样品为b处溶液. |
| 先产生气泡,后产生白色沉淀 | 该样品为c处溶液,并可推知溶液中的阳离子有Ca2+、H+. |
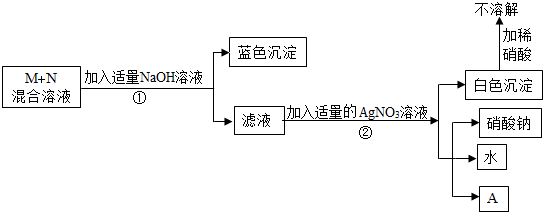
19.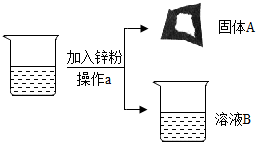 某工厂排故的废水中含有AgNO3、Cu(NO3)2和Al(NO3)3,某校化学兴趣小组的同学取了一瓶废水样品带回实验室进行实验.将废水静置后,取上层清液,加入锌粉.待充分反应后,得到固体A和溶液B.由图一可知,操作a的名称是过滤.
某工厂排故的废水中含有AgNO3、Cu(NO3)2和Al(NO3)3,某校化学兴趣小组的同学取了一瓶废水样品带回实验室进行实验.将废水静置后,取上层清液,加入锌粉.待充分反应后,得到固体A和溶液B.由图一可知,操作a的名称是过滤.
化学兴趣小组的同学对固体A的成分进行了探究,请你一起参与(不考虑杂质干扰)
【提出问题】固体A的成分是什么?
【猜想与假设】甲同学认为固体A是银;同学认为固体A是银和铜;丙同学认为固体A是银、铜、铝,你认为固体A还可能是银、铜、锌.
大家经过讨论后,认为丙同学的猜想错误,理由是铝比锌活泼,锌不能和硝酸铝反应.
【实验探究】设计实验探究固体A的成分,请填写表中空白:
由实验可知,固体A一定是银和铜.
【反思交流】若实验1观察到下列现象:
固体A$\stackrel{取样,滴加稀盐酸}{→}$无色气体
则溶液B中溶质的成分为硝酸锌和硝酸铝;写出产生气体反应的化学方程式Zn+2HCl═ZnCl2+H2↑.
 某工厂排故的废水中含有AgNO3、Cu(NO3)2和Al(NO3)3,某校化学兴趣小组的同学取了一瓶废水样品带回实验室进行实验.将废水静置后,取上层清液,加入锌粉.待充分反应后,得到固体A和溶液B.由图一可知,操作a的名称是过滤.
某工厂排故的废水中含有AgNO3、Cu(NO3)2和Al(NO3)3,某校化学兴趣小组的同学取了一瓶废水样品带回实验室进行实验.将废水静置后,取上层清液,加入锌粉.待充分反应后,得到固体A和溶液B.由图一可知,操作a的名称是过滤.化学兴趣小组的同学对固体A的成分进行了探究,请你一起参与(不考虑杂质干扰)
【提出问题】固体A的成分是什么?
【猜想与假设】甲同学认为固体A是银;同学认为固体A是银和铜;丙同学认为固体A是银、铜、铝,你认为固体A还可能是银、铜、锌.
大家经过讨论后,认为丙同学的猜想错误,理由是铝比锌活泼,锌不能和硝酸铝反应.
【实验探究】设计实验探究固体A的成分,请填写表中空白:
| 实验步骤 | 现象 |
| 实验1:取固体A加入盐酸 | 无气体产生 |
| 实验2:取溶液B加入 氢氧化钠溶液 | 无蓝色沉淀 |
【反思交流】若实验1观察到下列现象:
固体A$\stackrel{取样,滴加稀盐酸}{→}$无色气体
则溶液B中溶质的成分为硝酸锌和硝酸铝;写出产生气体反应的化学方程式Zn+2HCl═ZnCl2+H2↑.